
| A. | -46 kJ/mol | B. | -92 kJ/mol | C. | +92 kJ/mol | D. | +1800kJ/mol |
分析 旧键断裂吸收的能量减去新键生成释放的能量值即为反应热,1molN2含有1molN≡N,1molH2含有1molH-H,1molNH3含有3molN-H,依据△H=反应物的总键能-生成物的总键能进行计算.
解答 解:已知:N≡N键的键能为946kJ/mol,H-H键能为436kJ/mol,N-H键键能为391kJ/mol,反应热△H=反应物的总键能-生成物的总键能,对于反应2NH3(g)?N2(g)+3H2(g)的△H,1molN2含有1molN≡N,1molH2含有1molH-H,1molNH3含有3molN-H,故△H=2×3×391-946kJ/mol-3×436kJ/mol=+92kJ/mol,
故选C.
点评 本题考查反应热的有关计算,掌握反应热与键能的关系是解答关键,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质硼 | |
| 熔点/℃ | 810 | 710 | 180 | -68 | 2300 |
| 沸点/℃ | 1 465 | 1 418 | 160 | 57 | 2 500 |
| A. | SiCl4是分子晶体 | B. | 单质硼可能是原子晶体 | ||
| C. | AlCl3加热能升华 | D. | NaCl的键的强度比MgCl2的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断钠和镁的金属性强弱 | |
| B. | 铁投入CuSO4溶液中置换出铜,判断铜与铁的金属性强弱 | |
| C. | 酸性H2CO3<HCl,判断氯与碳的非金属性强 | |
| D. | F2与Cl2分别与足量的H2反应的难易,判断氟与氯的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为s轨道的形状是球形的,所以s电子做的是圆周运动 | |
| B. | 3px、3py、3pz的差异之处在于三者中电子(基态)的能量不同 | |
| C. | 原子轨道和电子云都是用来形象地描述电子运动状态的 | |
| D. | 电子云图上的每一个点都代表一个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
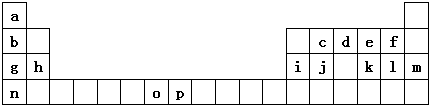
| 元素 | O | p | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
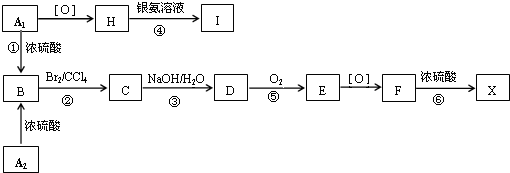
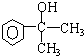 ;F
;F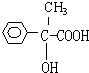 .
. ;
; .
. 、
、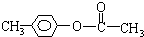 、
、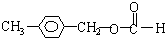 、
、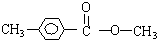 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com