
【题目】下列反应的离子方程式书写正确的是()
A. 氧化铜与稀硝酸反应:CuO + 2H+ ![]() Cu2+ + H2O
Cu2+ + H2O
B. 稀 H2SO4与铁粉反应:2Fe + 6H+ ![]() 2Fe3+ + 3H2↑
2Fe3+ + 3H2↑
C. 盐酸滴在石灰石上:2H++ CO32— ![]() H2O +CO2↑
H2O +CO2↑
D. 硫酸氢钠与过量氢氧化钡反应:Ba2++2OH—+ 2H+ +SO42—![]() BaSO4↓+ 2H2O
BaSO4↓+ 2H2O
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol,它由两步反应组成:
i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ/mol
ii.SO3(g)分解.
(1)SO3(g)分解的热化学方程式为
(2)工业上常用SO2制备Na2S2O3 , 向0.1mol/L的Na2S2O3溶液中滴加稀硫酸的离子方程式为 .
(3)反应ii的△S0 (填“>”、“<”、“=”).
(4)对反应ii,可用V2O5作催化剂. 已知:SO2+V2O5SO3+V2O4K1、 ![]() O2+V2O4V2O5K2 , 则在相同温度下,2SO3(g)2SO2(g)+O2(g)的平衡常数 K=(用K1、K2表示).
O2+V2O4V2O5K2 , 则在相同温度下,2SO3(g)2SO2(g)+O2(g)的平衡常数 K=(用K1、K2表示).
(5)L(L1、L2),X可分别代表压强或温度,如图表示L一定时,反应ii中SO3(g)的平衡转化率随X的变化关系. 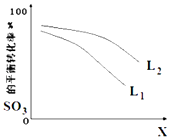
①X代表的物理量是;
②比较L1、L2的大小 .
(6)维持体系总压p恒定,在T℃时,物质的量为9mol、体积为2L的SO3(g)发生反应:2SO3(g)2SO2(g)+O2(g),已知SO3的平衡转化率25%,则在该温度下反应的平衡常数K=(用最简分数表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在50mL NaNO3和Na2SO4的混合溶液中,c (Na+)=1mol/L,往其中加入适量BaCl2溶液恰好完全反应,得到2.33g白色沉淀,则原混合溶液中c (NO3﹣)=mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1 molL-1的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
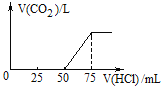
(1)A溶液中的溶质为_________(化学式),其物质的量之比是_______。
(2)通入CO2气体体积__________________(标准状况)。
(3)NaOH溶液的物质的量浓度______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离出来的c(H+)=1×10-13mol/L,该溶液可能是( )
①二氧化硫水溶液;②氯化铵水溶液;③硝酸钠水溶液;④氢氧化钠水溶液
A.①④B.①②C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL 0.1000molL﹣1 (NH4)2SO4溶液中逐滴加入0.2000molL﹣1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发).下列说法正确的是( ) 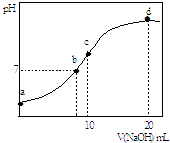
A.点a所示溶液中:c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH﹣)
C.点d所示溶液中:c(SO42﹣)>c(NH3H2O )>c(OH﹣)>c(NH4+)
D.点c所示溶液中:c(SO42﹣)+c(H+)=c(NH3H2O )+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于容量瓶及其使用方法的叙述,正确的是
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
A. ①和③ B. ①②④ C. 除了③ D. 除了⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下、0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后(假设混合液体积为二者之和),所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( ) 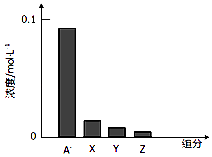
A.HA是弱酸
B.该混合液pH>7
C.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH﹣ , Z表示H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com