
| A. | 向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ | |
| B. | 碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | 盐酸跟氢氧化镁反应:H++OH-═H2O | |
| D. | 碳酸镁跟硫酸反应:MgCO3+H+═Mg2++H2O+CO2↑ |
分析 A.反应生成硝酸和氯化银;
B.反应生成氯化钙、水、二氧化碳,碳酸氢钙完全电离出钙离子和碳酸氢根离子;
C.氢氧化镁在离子反应中保留化学式;
D.电荷不守恒.
解答 解:A.向硝酸银溶液中加盐酸的离子反应为Ag++Cl-═AgCl↓,故A正确;
B.碳酸氢钙溶液跟盐酸反应的离子反应为HCO3-+H+═CO2↑+H2O,故B错误;
C.盐酸跟氢氧化镁反应的离子反应为2H++Mg(OH)2═Mg2++2H2O,故C错误;
D.碳酸镁跟硫酸反应的离子反应为MgCO3+2H+═Mg2++H2O+CO2↑,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意电荷守恒及离子反应中保留化学式的物质,题目难度不大.


科目:高中化学 来源: 题型:解答题
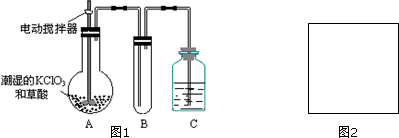 X+5H2O,则X的化学式NaCl.
X+5H2O,则X的化学式NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存FeCl2溶液时,通常在溶液中加少量的单质铁 | |
| B. | 常温下,浓硝酸可以用铁罐车贮运 | |
| C. | 可用湿润的蓝色石蕊试纸检验氨气 | |
| D. | 除去CO2中混有的HCl,可通过盛有饱和NaHCO3溶液的洗瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L -1 NaHC2O4溶液与0.1 mol•L -1KOH溶液等体积混合,所得溶液中:c(Na+)>c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-) | |
| B. | 20mL 0.1 mol•L -1NH4Cl溶液与10mL 0.1 mol•L -1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) | |
| C. | 常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:c(Na+)+c(OH-)>c(H+)+c(F-) | |
| D. | 0.1 mol•L -1NH3•H2O溶液与0.1 mol•L -1HNO3溶液等体积混合,所得溶液中:c(H+)>c(OH-)+c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应②中Cu2S只发生了氧化反应 | |
| B. | 反应①中氧化产物只有SO2 | |
| C. | 若1molCu2S完全转化为2molCu,则转移电子数为2NA | |
| D. | 将1molCu2S冶炼成2molCu,需要O21mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黏土 | B. | 纯碱 | C. | 石灰石 | D. | 熟石灰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com