
【题目】下列关于有机物的说法正确的是( )
A. 乙醇难溶于水 B. 乙烯可使酸性KMnO4溶液褪色
C. 乙酸的酸性比碳酸弱 D. 苯不能萃取碘水中的碘单质
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】己知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如下图所示。下列说法不正确的是( )

A. 0~a间发生反应:3HSO3-+IO3-=3SO42-+I-+3H+
B. a~b间共消耗NaHSO3的物质的量为1.8mol
C. b~c间反应:I2仅是氧化产物
D. 当溶液中I-与I2的物质的量之比为5∶3时,加入的KIO3为1.08mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的.下列环境问题与所对应的物质不相关的是( )
A.温室效应﹣﹣CO2
B.光化学污染﹣﹣NO2
C.酸雨﹣﹣SO2
D.臭氧层破坏﹣﹣CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠与水反应的改进实验操作如下:取一张滤纸,用酚酞试液浸润并晾干,裁剪并折叠成信封状,滤纸内放一小块(约绿豆粒般大小)金属钠,把含钠的滤纸信封放入水中,装置如下图所示。

请回答:
(1)写出金属钠与水反应的离子方程式________________。
(2)实验过程中取用金属钠的操作方法是________________。
(3)有关此实验的说法正确的是________________。
A.实验过程中,可能听到爆鸣声
B.实验过程中,看到滤纸信封由白色逐渐变红色
C.实验改进的优点之一是由实验现象能直接得出反应产物
D.实验过程中,多余的金属钠不能放回原试剂瓶中,以免对瓶内试剂产生污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期VA族。D、E、H均为难溶于水的白色固体:化合物C、E均含A元素。其余物质均为中学化学中常见物质。
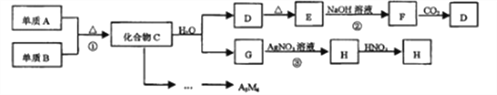
请回答:
(1)写出H的化学式:________________。
(2)化合物A3M4中含有的化学键类型为:________________。
(3)写出反应②的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是( )

A. 图(a)所示电池中,MnO2的作用是催化剂
B. 图(b)所示电池放电过程中,硫酸浓度不断增大
C. 图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、氧、铝都为重要的短周期元素,其单质及化合物在工农业生产生活中有重要作用。请回答下列问题:
(1)在密闭容器内(反应过程保持体积不变),使1molN2和3molH2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。当反应达到平衡时,N2和H2的浓度之比是_______;当升高平衡体系的温度,则混合气体的平均式量______(将“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1mol N2,H2的转化率_______(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡_______移动(填“正向”“逆向”或“不”)。
2NH3(g) △H=-92.4kJ/mol。当反应达到平衡时,N2和H2的浓度之比是_______;当升高平衡体系的温度,则混合气体的平均式量______(将“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1mol N2,H2的转化率_______(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡_______移动(填“正向”“逆向”或“不”)。
(2)由题干所述元素中的三种组成的某种强酸弱碱盐的化学式为________,其溶于水能_____水的电离(填“促进”或“抑制”),且使溶液的pH_______(填“升高”“降低”或“不变”),原因是_________(用离子方程式表示)。
(3)空气是硝酸工业生产的重要原料,氨催化氧化是硝酸工业的基础,氨气在铁触媒作用下只发生主反应①和副反应②:
4NH3(g)+5O2![]() 4NO+6H2O(g) △H=-905kJ/mol ①
4NO+6H2O(g) △H=-905kJ/mol ①
4NH3(g)+3O2![]() 2N2+6H2O(g) △H=-1268kJ/mol ②
2N2+6H2O(g) △H=-1268kJ/mol ②
①氮气与氧气反应生成NO的热化学方程式为______________________。
②在氧化炉中催化氧化时,有关物质的产率与温度的关系如图。下列说法中正确的是_____。

A.工业上氨催化氧化生成NO时,最佳温度应控制在780~840℃之间
B.工业上采用物料比![]() 在1.7~2.0,主要是为了提高反应速率
在1.7~2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.由图可知,温度高于900℃时,生成N2的副反应增多,故NO产率降低
(4)M是重要的有机化工原料,其分子与H2O2含有相同的电子数,将1molM在氧气中完全燃烧,只生成1molCO2和2molH2O,则M的化学式为_______。某种燃料电池采用铂作为电极催化剂,以KOH溶液为电解质,以M为燃料,以空气为氧化剂。若该电池工作时消耗1molM,则电路中通过_____mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水溶液一定呈中性的是
A. c(NH4+)=c(C1-)的NH4Cl 溶液
B. c(H+)=1×10-7mol·L-1的溶液
C. pH=7的溶液
D. 室温下将pH=3的酸与pH= 11的碱等体积混合后的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com