
【题目】据报道,某国一集团拟在太空建造巨大的激光装置,把太阳光变成激光用于分解海水制氢:2H2O![]() 2H2↑+O2↑,下列说法正确的是( )
2H2↑+O2↑,下列说法正确的是( )
①水的分解反应是放热反应
②氢气是一级能源
③使用氢气作燃料有助于控制温室效应
④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可以改善生存环境
A. ①② B. ②③ C. ①③ D. ③④
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列说法不正确的是 ( )
A. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C. “甘之如饴”说明糖类均有甜味
D. 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
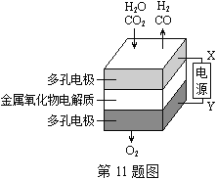
A.X是电源的负极
B.阴极的反应式是:H2O+2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ
C.总反应可表示为:H2O+CO2![]() H2+CO+O2
H2+CO+O2
D.阴、阳两极生成的气体的物质的量之比是1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将金属钠放在燃烧匙中在空气中加热使其燃烧,不可能出现的现象是( )
A.金属钠熔化为小球
B.火焰为黄色
C.燃烧后得到一白色固体
D.燃烧后得到淡黄色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯从1902年开始研究由氮气和氢气直接合成氨。合成氨是人类科学技术上的一项重大突破,其反应原理为: N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
一种利用天然气合成氨的简易流程如下:
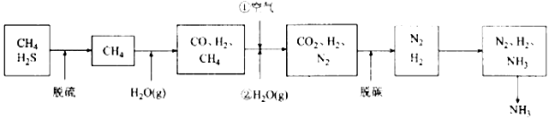
天然气先经脱硫,然后通过两次转化,再经过二氧化碳脱除等工序,得到氮氢混合气,进入氨合成塔,制得产品氨。
(1)仅从提高氨产率的角度,氨合成塔中适宜的生产条件是 。
(2)CH4与水蒸气制氢气的反应为CH4(g)+ H2O (g)![]() CO (g) +3H2(g),在2 L的密闭容器中,将物质的量各1 mol的CH4和H2O (g)混合反应,CH4的平衡转化率与温度、压强的关系如下图所示:
CO (g) +3H2(g),在2 L的密闭容器中,将物质的量各1 mol的CH4和H2O (g)混合反应,CH4的平衡转化率与温度、压强的关系如下图所示:
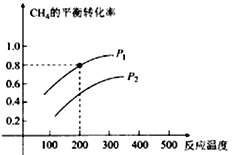
①该反应的△H 0(填﹥、﹤)。
②图中压强P1 P2(填﹥、﹤)。
③200℃时该反应的平衡常数K= (保留一位小数)。
(3)NH3经过催化氧化生成NO,以NO为原料通过电解的方法可以制备NH4NO3,其总反应是8NO+7H2O ![]() 3NH4NO3+2HNO3,试写出以惰性材料作电极的阴极反应式: ;阳极反应式: ;电解过程中需要补充一种物质才能使电解产物全部转化为NH4NO3,该物质是 。
3NH4NO3+2HNO3,试写出以惰性材料作电极的阴极反应式: ;阳极反应式: ;电解过程中需要补充一种物质才能使电解产物全部转化为NH4NO3,该物质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.硫酸氢铵溶液中滴加少量NaOH溶液:H++OH-=H2O
B.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32—+H2O
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+CO32-
D.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42﹣、CO32﹣
B.在含大量Ba2+的溶液中:NH4+、Na+、Cl﹣、NO3﹣
C.在强碱溶液中:Na+、K+、Cl﹣、HCO3﹣
D.在pH=1的溶液中:K+、Fe2+、Cl﹣、CH3COO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡 的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡 的1.8倍,下列叙述正确的是
A.a<c+d B.A的转化率增大
C.D的体积分数变大 D.平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+8NH3![]() 7N2+12H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是________L。
7N2+12H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是________L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1
2NO(g)+O2(g)2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=___________kJ·mol-1。
SO3(g)+NO(g)的ΔH=___________kJ·mol-1。
一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1molSO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=___________。
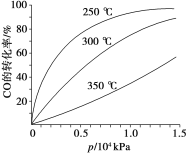
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应ΔH___________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是__________________________。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应ΔH___________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com