
����Ŀ���¹���ѧ�ҹ�����1902�꿪ʼ�о��ɵ���������ֱ�Ӻϳɰ����ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ�� N2(g)+3H2(g)![]() 2NH3(g) ��H=��92.4kJ��mol��1
2NH3(g) ��H=��92.4kJ��mol��1
һ��������Ȼ���ϳɰ��ļ����������£�
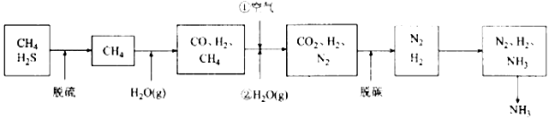
��Ȼ���Ⱦ�����Ȼ��ͨ������ת�����پ���������̼�ѳ��ȹ��õ��������������백�ϳ������Ƶò�Ʒ����
��1��������߰����ʵĽǶȣ����ϳ��������˵����������� ��
��2��CH4��ˮ�����������ķ�ӦΪCH4(g)+ H2O (g)![]() CO (g) +3H2(g)����2 L���ܱ������У������ʵ�����1 mol��CH4��H2O (g)��Ϸ�Ӧ��CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CO (g) +3H2(g)����2 L���ܱ������У������ʵ�����1 mol��CH4��H2O (g)��Ϸ�Ӧ��CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
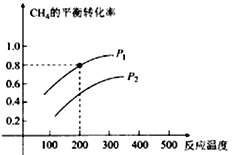
�ٸ÷�Ӧ����H 0�����������
��ͼ��ѹǿP1 P2�����������
��200��ʱ�÷�Ӧ��ƽ�ⳣ��K= ������һλС������
��3��NH3��������������NO����NOΪԭ��ͨ�����ķ��������Ʊ�NH4NO3�����ܷ�Ӧ��8NO+7H2O ![]() 3NH4NO3+2HNO3����д���Զ��Բ������缫��������Ӧʽ�� ��������Ӧʽ�� ������������Ҫ����һ�����ʲ���ʹ������ȫ��ת��ΪNH4NO3���������� ��
3NH4NO3+2HNO3����д���Զ��Բ������缫��������Ӧʽ�� ��������Ӧʽ�� ������������Ҫ����һ�����ʲ���ʹ������ȫ��ת��ΪNH4NO3���������� ��
���𰸡���1�����¡���ѹ��2���٣��ڣ���K=69.1��mol��L��1��2
��3��������3NO+15e-+18H+=3NH4++3H2O
������5NO��15e-+10H2O=5NO3-+20H+����ˮ����
��������
�����������1����Ϊ�ϳɰ��ķ�ӦΪ�����С�ķ��ȷ�Ӧ��Ϊ��߰���������ƽ�������ƶ������ϳ��������˵�������������������ѹ��
��2������ͼ��֪��ѹǿ���䣬�¶�Խ��CH4��g����ת����Խ���¶�����ƽ��������Ӧ�����ƶ��������¶�ƽ�������ȷ�Ӧ�����ƶ�����������ӦΪ���ȷ�Ӧ������H��0�� ���¶��ݻ����䣬����ѹǿƽ���������С�ķ����ƶ����淴Ӧ�����ƶ�����CH4��g����ת����ԽС������ѹǿԽ��CH4��g����ת����ԽС����P1��P2����200�棬CH4��g����ת����0.8�����Բμӷ�Ӧ��CH4��g�������ʵ���Ϊ0.8mol��
CH4��g��+H2O��g���TCO��g��+3H2��g��
��ʼŨ����mol/L����0.5 0.5 0 0
ת��Ũ����mol/L����0.4 0.4 0.4 1.2
ƽ��Ũ����mol/L����0.1 0.1 0.4 1.2
����200��ʱ�÷�Ӧ��ƽ�ⳣ��K= c(CO)c3(H2)/ c(CH4)c(H2O) =(0.4��1.23)/(0.1��0.1)=69.1��mol��L��1��2��
��3�����NO�Ʊ�NH4NO3������������ԭ��Ӧ���缫��ӦʽΪ3NO + 15e-+ 18H+ = 3NH4+ + 3H2O����������������Ӧ���缫��ӦʽΪ5NO��15e- + 10H2O = 5NO3-+20 H+����������Ӧ�ɿ�����Ҫʹ��ʧ�����غ㣬����������NO3-�����ʵ�����������������NH4+�����ʵ������ܷ�Ӧ����ʽΪ8NO+7H2O ![]() 3NH4NO3+2HNO3�������Ҫʹ������ȫ��ת��ΪNH4NO3���貹��������ˮ��
3NH4NO3+2HNO3�������Ҫʹ������ȫ��ת��ΪNH4NO3���貹��������ˮ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�������ԭ��������ǣ��������õ�����ڵ��Ȼ����ķ�������ȡ������ �������Ƽ����Ȼ�þ������Һ����ȡþ �����ȷֽⷨұ���� ��ʪ����ͭ����п������ͭ��Һ��Ӧ�û���ͭ
A���ڢ� B���٢� C���٢ڢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
A. ��BaCl2��Һ�м�������Na2CO3��Һ���ã����ϲ���Һ�м����μ�Na2CO3��Һ����������˵��Ba2���Ѿ���ȫ����
B. ������ϡ�����������ˮ���NaOH��Һʹ��Һ�ʼ��ԣ���������Cu��OH��2�����ȣ����к�ɫ�������ɣ�˵�������Ѿ���ȫˮ��
C. ��Na2SO4��10H2O�������������м��ȣ���ȴ����������ظ��������������������γ����Ľ����ͬ��˵����������ȫ��ʧȥ�ᾧˮ
D. ����ʽ�ζ�������з�̪��NaOH��Һ�еμӱ�HCl��Һ�����������һ��HCl��Һ��ۺ�ɫ�պ���ȥ��˵���Ѵ�ζ��յ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ת��Ҫ���뻹ԭ������ʵ�ֵ��ǣ� ��
A.SO32����SO2
B.SO2��S
C.Fe2+��Fe3+
D.Cl2��ClO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������л�Ϊͬϵ�����
A�������Ǻ����� B�����Ǻ���ѿ��
C������ͱ�����CH3CH2COOH�� D���Ҵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ�����ij��һ��������̫�ս����ļ���װ�ã���̫�����ɼ������ڷֽ⺣ˮ���⣺2H2O![]() 2H2��+O2��������˵����ȷ����( )
2H2��+O2��������˵����ȷ����( )
��ˮ�ķֽⷴӦ�Ƿ��ȷ�Ӧ
��������һ����Դ
��ʹ��������ȼ�������ڿ�������ЧӦ
���������ɵ�����������ж���Ķ�����̼��Ӧ���ɼ״��������������Ը������滷��
A. �٢� B. �ڢ� C. �٢� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20mL0.1mol/LBaCl2��Һ��Cl�������ʵ���Ũ��= �� Ba2+�����ʵ���= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ��ԭ�ӵĺ����������ܲ㣬�����ܲ���4�����ӣ���ԭ�Ӻ��ڵ�������Ϊ (����)
A. 14 B. 15 C. 16 D. 17
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƿ�Ӧ��2SO2��O2![]() 2SO3�ڲ�ͬ�����´ﵽƽ��״̬ʱSO2��ת���ʡ�
2SO3�ڲ�ͬ�����´ﵽƽ��״̬ʱSO2��ת���ʡ�
ѹǿ ת���� �¶� | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
400�� | 99.2% | 99.6% | 99.7% | 99.9% |
500�� | 93.5% | 96.9% | 97.8% | 99.3% |
600�� | 73.7% | 85.8% | 89.5% | 96.4% |
�Իش��������⡣
(1)���ڿ��淴Ӧ���ȣ����ܵó�ʲô��ʾ��
________________________________________��
(2)��߸û�ѧ��Ӧ�ȵ�;���У�_____________________��
(3)Ҫʵ��SO2��ת����Ϊ93.5%������Ƶķ�Ӧ������____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com