
【题目】下列化工生产原理错误的是:①可以用电解熔融的氯化铝的方法来制取金属铝 ②可以把钠加入氯化镁饱和溶液中制取镁 ③用热分解法冶炼铁 ④湿法炼铜是用锌和硫酸铜溶液反应置换出铜
A.②③ B.①③ C.①②③ D.①②③④
科目:高中化学 来源: 题型:
【题目】某天然碱样品的组成可能为aNa2CO3bNaHCO3cH2O(a、b、c为正整数)。为确定其组成,某小组进行如下实验:
(1)定性实验
①取少量天然碱样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝。___________(填“能”或“不能”)说明样品中含结晶水,试简述理由 ;
②请设计一个简单方案,确认样品中含有CO32- 。
(2)定量分析
该同学设计了如下图所示装置,测定天然碱的化学组成。
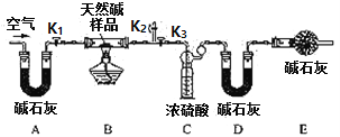
实验步骤:
①组装好实验装置后,首先进行的操作是 ;A处碱石灰的作用是;E处碱石灰的作用是 。
②称7.3g样品,放入硬质玻璃管中;称量C装置质量为87.6g,D装置为74.7g。
③打开活塞K1、K2,关闭K3,通入空气数分钟。
④关闭活塞Kl、K2,打开K3,点燃酒精灯至不再产生气体为止。
⑤打开活塞Kl,鼓入空气数分钟,然后称得C装置质量为88.5g;D装置质量为75.8g,通入空气的目的是 。
⑥如果a=1,则该天然碱的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了高热值的煤炭气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。生产煤炭气的反应之一是:
C(s)+H2O(g)![]() CO(g)+H2(g)ΔH=+131.4kJ/mol
CO(g)+H2(g)ΔH=+131.4kJ/mol
(1)在容积为3 L的密闭容器中发生上述反应,5 min后容器内气体的密度增大了0.12 g/L,用H2O表示0 ~ 5 min的平均反应速率为______________________。
(2)关于上述反应在化学平衡状态时的描述正确的是 。
A.CO的含量保持不变
B.v正(H2O)= v正(H2)
C.容器中混合气体的平均相对分子质量保持不变
(3)若上述反应在t0时刻达到平衡(如图),在t1时刻改变某一条件,请在右图中继续画出t1时刻之后正反应速率随时间的变化:
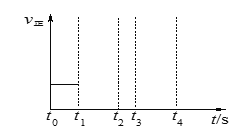
①缩小容器体积,t2时到达平衡(用实线表示);
②t3时平衡常数K值变大,t4到达平衡(用虚线表示)。
(4)在一定条件下用CO和H2可以制得甲醇,CH3OH和CO的燃烧热为别725.8 kJ/mol ,283.0 kJ/mol,水的摩尔蒸发焓为44.0 kJ/mol,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式: 。
(5)如下图所示,以甲醇燃料电池作为电源实现下列电解过程。乙池中发生反应的离子方程式为 。当甲池中增重16 g时,丙池中理论上产生沉淀质量的最大值为 g。
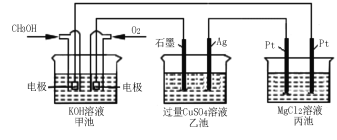
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 苯和苯酚都属于芳香烃
B. CCl4可由CH4制得,可萃取碘水中的碘
C. 硝化甘油、TNT都是硝酸酯
D. 石油主要是各种烷烃、环烷烃、烯烃组成的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:H2(g) + I2(g) ![]() 2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深
D.容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列说法不正确的是 ( )
A. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C. “甘之如饴”说明糖类均有甜味
D. 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种固态物质熔化或升华时,克服的微粒间相互作用力属于同种类型的是( )
A. 碘和氯化钾 B. 金刚石和重晶石
C. 二氧化硅和干冰 D. 二氧化碳和甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香族化合物甲的分子式为C10H11ClO2,已知苯环上只有两个取代基,其中一个取代基为—Cl,甲能与饱和碳酸氢钠溶液反应放出二氧化碳,则满足上述条件的有机物甲的同分异构体数目有多少种
A. 5种 B. 9种 C. 12种 D. 15种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯从1902年开始研究由氮气和氢气直接合成氨。合成氨是人类科学技术上的一项重大突破,其反应原理为: N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
一种利用天然气合成氨的简易流程如下:
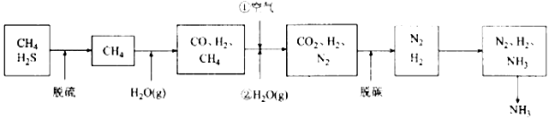
天然气先经脱硫,然后通过两次转化,再经过二氧化碳脱除等工序,得到氮氢混合气,进入氨合成塔,制得产品氨。
(1)仅从提高氨产率的角度,氨合成塔中适宜的生产条件是 。
(2)CH4与水蒸气制氢气的反应为CH4(g)+ H2O (g)![]() CO (g) +3H2(g),在2 L的密闭容器中,将物质的量各1 mol的CH4和H2O (g)混合反应,CH4的平衡转化率与温度、压强的关系如下图所示:
CO (g) +3H2(g),在2 L的密闭容器中,将物质的量各1 mol的CH4和H2O (g)混合反应,CH4的平衡转化率与温度、压强的关系如下图所示:
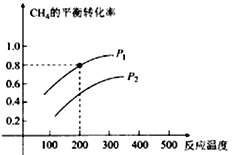
①该反应的△H 0(填﹥、﹤)。
②图中压强P1 P2(填﹥、﹤)。
③200℃时该反应的平衡常数K= (保留一位小数)。
(3)NH3经过催化氧化生成NO,以NO为原料通过电解的方法可以制备NH4NO3,其总反应是8NO+7H2O ![]() 3NH4NO3+2HNO3,试写出以惰性材料作电极的阴极反应式: ;阳极反应式: ;电解过程中需要补充一种物质才能使电解产物全部转化为NH4NO3,该物质是 。
3NH4NO3+2HNO3,试写出以惰性材料作电极的阴极反应式: ;阳极反应式: ;电解过程中需要补充一种物质才能使电解产物全部转化为NH4NO3,该物质是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com