


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源:不详 题型:单选题
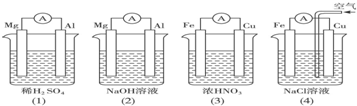
| A.(1)(2)中Mg作负极,(3)(4)中Fe作负极 |
| B.(2)中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑ |
| C.四个装置中某一电极上均有气泡产生 |
| D.(4)中Cu作正极,电极反应式为2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)分析如图所示的四个装置,回答下列问题:

①装置a和b中铝电极上的电极反应式分别为_____________________________、_____________________________________________。
②装置c中产生气泡的电极为________电极(填“铁”或“铜”),装置d中铜电极上的电极反应式为__________________________________________________。
(2)观察如下图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为___________________、____ ____________。
 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com