
【题目】电解饱和食盐水的阳极产物是
A. NaOH B. H2 C. HCl D. Cl2
科目:高中化学 来源: 题型:
【题目】石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。

实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(1) 装置A的作用是______________________________;
(2) 试管①中发生的主要反应有:
C17H36![]() C8H18+C9H18C8H18
C8H18+C9H18C8H18![]() C4H10+C4H8
C4H10+C4H8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_________和________,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于______反应。其可能结构为______(填序号)

(3)写出试管③中反应的一个化学方程式_____________________________,该反应的类型为__________反应。
(4)试管②中的少量液体的组成是____________(填序号)
A.甲烷B.乙烯C.液态烷烃D.液态烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图表法、图像法是常用的科学研究方法。
下表列出原子序数依次增大的短周期元素中四种元素性质的一些数据:
性质 元素 | A | B | C | D |
原子半径(10-10 m) | 0.37 | 0.77 | 0.74 | 0.99 |
最高价态 | +1 | +4 | - | +7 |
最低价态 | -1 | -4 | -2 | -1 |
用所给元素试回答下列问题:
(1)比元素A原子序数大28的元素,其基态原子的核外电子排布式为___________。
(2)元素A、B、C可形成一种相对分子质量为60的一元羧酸分子,则一个该分子中共含有________个σ键,________个π键。
(3)如图是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第________族元素氢化物的沸点的变化规律。(2分)
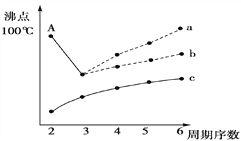
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是________,理由是__________________________________(2分)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将气体X、Y放入密闭容器中发生反应生成Z,5min后达到平衡。其初始浓度和平衡浓度如下表:下列说法错误的是
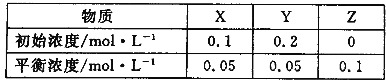
A.该反应可表示为 X+3Y![]() 2Z
2Z
B.反应达到平衡时,X的转化率为50%
C.前5min 以Y表示的平均反应速率为υ(Y)= 0.01 mol·L-1·min-1
D.增大压强使平衡向生成Z的方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物E具有抗癌抑菌功效,其合成路线如下。

已知:NaBH4是一种很强的还原剂,可以将 —C≡N还原为 —CH2NH2
(1)化合物A的含氧官能团有____________;A的同分异构体中含有结构:![]() 、-CH2CH(NH2)COOH、-C4H9;且所有取代基都集中在同一苯环上的有____________种。
、-CH2CH(NH2)COOH、-C4H9;且所有取代基都集中在同一苯环上的有____________种。
(2)反应①实际经历了两步反应,这两步的反应类型依次为__________、__________;设计反应①和③的目的是____________________________________。
(3)关于化合物D的说法错误的是______________(填序号)。
A.1molD最多可与3molH2发生加成反应 B.可以与盐酸发生反应
C.可以使高锰酸钾酸性溶液褪色 D.是一种芳香烃
(4)反应物![]() 的名称为_______________;写出其与氧气等物质的量反应的化学方程式__________________________________________________________________;
的名称为_______________;写出其与氧气等物质的量反应的化学方程式__________________________________________________________________;
(5)阅读以下信息,依据以上流程图和所给信息,以CH3CHO和CH3NH2为原料设计合成丙氨酸【CH3CH(NH2)COOH】的路线。______________________________________已知:

提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A. 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2NA
B. 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA
C. 标准状况下,44.8L NO与22.4 L O2反应后的分子数是2NA
D. 27g铝中加入1mol/L的NaOH溶液,转移电子数是3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
试验编号 | HX的物质的量浓度(mol/L) | NaOH的物质的量浓度(mol/L) | 混合溶液的PH |
甲 | 0.2 | 0.2 | PH=a |
乙 | c1 | 0.2 | PH=7 |
丙 | 0.2 | 0.2 | PH>7 |
丁 | c2 | c3 | PH=10 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a________7(填“>”“<”或“=”),则HX为强酸;若a________7(填“>”“<”或“=”),则HX为弱酸.
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是________.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)丙溶液中离子浓度由大到小的顺序是_____________________________.
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷、乙烯、乙炔它们及其衍生物一氯乙烷、氯乙烯、乙醇、乙醛、乙酸、乙酸乙酯都有很重要的用途。
(1)乙炔在空气中燃烧的现象____________________________________________________
由乙烷制取一氯乙烷的反应条件___________________,由乙烯制取乙醇的反应类型_________
(2)一氯乙烷分子中的官能团为__________________。聚氯乙烯的结构简式为________________。
(3)写出由乙醛生成乙酸的化学反应方程式。__________________________________________
(4)写出乙酸的一种同分异构体的结构简式____________________________;检验该同分异构体是否含有醛基操作_________________________________________________________
______________________________________________________________
(5)乙二醇(HOCH2CH2OH)也是一种很重要的化工原料,请完成由一氯乙烷合成乙二醇的路线图(合成路线常用的表示方式为:![]() )
)
____________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com