
����Ŀ���������ⶨˮ���ܽ����ķ����ǣ�
����ȡa mLˮ����Ѹ�ټ���̶���MnSO4��Һ�ͼ���KI��Һ(��KOH)����������ƿ����������ʹ֮��ַ�Ӧ���䷴ӦʽΪ��2Mn2����O2��4OH��===2MnO(OH)2(�÷�Ӧ����)��
�ڲⶨ��������Ѹ�ټ���1��2 mLŨ����(�ữ���ṩH��)��ʹ֮����I2������b mol/L��Na2S2O3��Һ�ζ�(�Ե���Ϊָʾ��)������V mL���йط�ӦʽΪ��MnO(OH)2��2I����4H��===Mn2����I2��3H2O��I2��2S2O![]() ===2I����S4O
===2I����S4O![]() ��
��
�Իش�
��1���ζ��������õ��IJ�������������ʽ�ζ��ܡ���ʽ�ζ����ȱ��_____________��
��2���ζ�����ʱ�����ֿ��Ƶζ��ܣ�����________���۾�Ҫע��________��
��3��ˮ���ܽ����ļ���ʽ��______(��g/LΪ��λ)��
��4���ζ�(I2��S2O![]() ��Ӧ)�Ե���Ϊָʾ�����յ�ʱ��Һ��________ɫ��Ϊ________ɫ���Ұ�����ڲ���ɫ��
��Ӧ)�Ե���Ϊָʾ�����յ�ʱ��Һ��________ɫ��Ϊ________ɫ���Ұ�����ڲ���ɫ��
���𰸡� ��ƿ���ձ� ��������ƿ ��ƿ����Һ��ɫ�ı仯 8bV/a �� ��
�������������������1�������к͵ζ����������жϣ�
��2���ζ�ʱ�����ֿ��Ƶζ��ܻ����������ճ���ƿ���ߵα����۾�ע����ƿ����Һ��ɫ�ı仯��
��3�����ݹ�ϵʽ��O2��2MnO��OH��2��2I2��4S2O32-�ɼ���ˮ�����ܽ�����Ũ�ȣ���4������I2�ĵ�����Һ����ɫ������S2O32-����I2���յ�ʱI2��ȫ��Ӧ��
����������1���к͵ζ�ǰ����и����ݡ�����Ȳ��������ձ�ʢҺ�壬�ζ�������ƿʢ����Һ���õζ���ʢ��Һ��������ʽ�ζ��ܡ���ʽ�ζ����ȱ����ƿ���ձ�����2���ζ�ʱ�����ֿ��Ƶζ��ܻ����������ճ���ƿ���ߵα����۾�ע����ƿ����Һ��ɫ�ı仯����3��
���ݷ�Ӧ��2Mn2++O2+4OH-�T2MnO��OH��2�� MnO��OH��2+2I-+4H+�TMn2-+I2+3H2O��I2+2S2O32-�TS4O62-+2I-��
��֪��ϵʽ��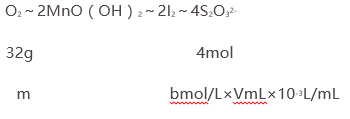
���m=8bV��10-3g����1Lˮ������������Ϊ�� ![]() g/L
g/L
��4������I2�ĵ�����Һ����ɫ������S2O32-����I2���յ�ʱI2��ȫ��Ӧ���յ�ʱ��Һ����ɫɫ��Ϊ��ɫɫ���Ұ�����ڲ���ɫ��


 �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�� A��B��C��D������ B2-������ C+���Ӻ��ⶼ�ж������Ӳ㣬B ԭ�ӵ��������� C ԭ�ӵ� ������֮�͵��� D ԭ�ӵ���������A ԭ��ʧȥһ�����Ӻ���һ�����ӣ��Իش�
(1)A��B��C��D ��Ԫ�ط��ŷֱ�Ϊ____��____��____��____��
(2)B2-�ĵ���ʽ ________��D ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ____��B �� C �γɵļ�����ĵ���ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݼ۲���ӶԻ���ģ�ͣ��ж����з��ӻ������ӵĿռ乹�Ͳ��������εģ�������
A. PCl3 B. H3O+ C. HCHO D. PH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ý���ʵ�飬�����������ƶϳ����۵��ǣ� ��
ѡ�� | �Լ�X | Y���Լ������� | ���� | װ�� |
A | һ���� | ��̪��Һδ��� | ���β���������� |
|
B | С�մ�ʹ��� | ʯ��ˮ����� | �����С�մ��ȶ� | |
C | �����������Ȼ�� | ��������Һ���Ȳ����������ܽ� | Ag2O�����ڰ�ˮ | |
D | �������������� | ���ۡ��⻯�غͺ�����Ļ����Һ���� | ��Ӧ������Cl2 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��298Kʱ����n(HA)+n(A��)=0.lmol��HA��NaA���������ˮ�γ�1L��Һ����Һ��c(HA)��c(A��)��pH�Ĺ�ϵ��ͼ��ʾ��������������ȷ����
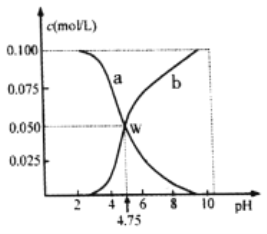
A. a�߱�ʾ����c(A��)�ı仯
B. pH=6 ʱ��c(Na+)+c(HA)>0. 1mol/L
C. 298Kʱ��A����ˮ��ƽ�ⳣ��(K)��������Ϊ10-10
D. ���������ʵ�����HA��NaA����ˮ�У�������ҺpHǡ��Ϊ4.75
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϱ���������ͭ����NO2��Ӧ��ijС�����������ʵ��װ�ý���̽����̽���������ijɷ֣����������N2����NO��
��֪������KMnO4��Һ������NO����NO3����
NO��FeSO4��Һ��Ӧ��NO+FeSO4=[Fe(NO)]SO4(��ɫ)��
Cu2O+2H+=Cu+Cu2++H2O
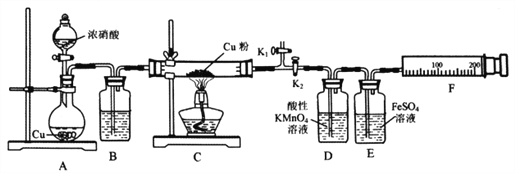
��ش��������⣺
��1��A�з�Ӧ�Ļ�ѧ����ʽΪ________________________��
��2�����װ�������ԣ�װ��ҩƷ��Ȼ��ʵ�����ȷ����˳����____________
���ر�K1����K2 ����Һ©������
����K1���ر�K2 ����ȼC���ƾ���
��3��ʵ������У�Dװ���е�������____________���ܷ����Dװ���е�����ȷ��C������NO����? ______��������________________________��
��4��Eװ�õ�������____________��
��5����ͭ����ȫ��Ӧ��ʵ��С��Է�Ӧ��Ĺ���ɷ�������²��룺��ֻ��CuO����ֻ��Cu2O����ͬѧ��Ϊ��ͨ���Ķ���ʵ�鼴���жϲ������Ƿ��������ʵ�鷽����_____________________��
��6��ʵ����Eװ����ʼ����δ����ɫ��С�����ͨ������ʵ��õ��������ݡ�
Cװ������ | Fװ����������(������Ϊ��״��) | ||
�������� | Cu���� | ��Ӧ��(����+������) | |
mg | 1.92g | (m+2.24)g | 112mL |
�ݴ�д��ʵ��ʱʵ�ʷ�����Ӧ�Ļ�ѧ����ʽ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������Һ�д���������ǣ�������
A.Ag+��K+��NO3����Cl��
B.Mg2+��Na+��Cl����SO42��
C.Ca2+��Mg2+��OH����Cl��
D.H+��Na+��CO32����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��84����Һ��ƿ�岿�ֱ�ǩ��ͼ��ʾ���á�84����Һ��ͨ��ϡ��100��(���֮��)��ʹ�á���ش��������⣺

��1���á�84����Һ�������ʵ���Ũ��ԼΪ__mol��L-1 ������1λС������
��2��ijͬѧȡ100mL�á�84����Һ����ϡ�ͺ�����������ϡ�ͺ����Һ��c(ClO-)_________mol��L-1(������ClO-��ˮ��)��
��3����ͬѧ���ĸá�84����Һ�����䷽������NaClO��������480mL��NaClO��������Ϊ25%������Һ������˵������ȷ����________������ĸ����
A������ͼ��ʾ�������У��������Dz���Ҫ�ģ�������Ҫһ�ֲ�������
B���������õ�NaClO�������ձ����ܽ��Ӧ����ת������ƿ
C������ʱ��������ƿ�̶��ᵼ��������ҺŨ��ƫ��
D����Ҫ����NaClO���������Ϊ149.0g
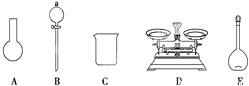
��4����ͬѧ������ƿ����ʹ�÷�������ʶ����ȷ����_______������ĸ����
A.����ƿ�ϱ����ݻ����¶Ⱥ�Ũ��
B.ʹ��ǰҪ�������ƿ�Ƿ�©Һ
C.����ƿ������ˮϴ�������ɺ���ʹ��
D.������Һ�����У�����ƿ��Һ��ֻ��Ҫһ��ҡ�ȹ���
��5����84����Һ����ϡ������ʹ�ÿ���ǿ����������ij����С����Ա��18.4mol��L-1 ��Ũ��������2L2.3molL��1��ϡ����������ǿ��84����Һ������������������Ũ��������Ϊ_____mL��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com