
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在 C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素的原子结构示意图为 。
②该金属元素的单质与某红色氧化物在高温下反应,可用于焊接铁轨及定向爆破,已知:1mol该单质完全反应,当温度恢复至298K时,共放热QkJ,请写出该反应的热化学反应方程式为 。
(2)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①用化学方程式表明B溶液呈碱性的原因 。
②自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100 mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为___________________。
(1)① ②2Al(s)+Fe2O3(s)
②2Al(s)+Fe2O3(s) Al2O3(s)+2Fe(s); △H=-2QkJ/mol
Al2O3(s)+2Fe(s); △H=-2QkJ/mol
(2)①CO32-+H2O OH-+ HCO3-
OH-+ HCO3-
② 2.65 g
解析试题分析:(1)①若A、B、C中均含同一种常见金属元素,将A、C的水溶液混合可得B的沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,x为氢氧化钠,因此可得出A中含金属元素Al的结构示意图。
②该金属元素的单质与某红色氧化物在高温下反应为铝与Fe2O3发生的铝热反应,配平后Al的系数为2,则△H=-2QkJ/mol,则人化学方程式为2Al(s)+Fe2O3(s) Al2O3(s)+2Fe(s); △H=-2QkJ/mol
Al2O3(s)+2Fe(s); △H=-2QkJ/mol
(2)①若A、B、C的焰色反应均呈黄色,水溶液均为碱性,则A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,x为二氧化碳。Na2CO3溶液呈碱性的原因是CO32?发生了水解反应,方程式为:CO32-+H2O OH-+ HCO3-。
OH-+ HCO3-。
②溶液中金属阳离子的浓度为0.5 mol?L?1,即钠离子浓度为0.5mol/L.取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为1/2×0.1L×0.5mol/L×106g/mol=2.65g。
考点:本题考查元素化合物推断、结构示意图、方程式的书写以及相关计算。


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:填空题
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空: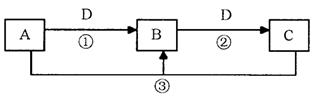
(1)若D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是 (只写一种)。
(2)若A是一种碱性气体,常用作制冷剂,B和D为空气的主要成分,则反应②的化学方程式为 。
(3)若D的氯碱工业的主要产品,B有两性,则反应②的离子方程式是 。
(4)若C是一种温室气体,D是空气的主要成分之一,1 mol黑色固体A完全燃烧放出393.5kJ热量,1 molB气体完全燃烧放出283.0kJ热量,则A→B反应的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有分子式为C10H10O2Br2的芳香族化合物X,X中苯环上有四个取代基,苯环上的一氯代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。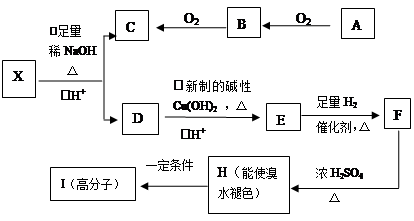
已知:
①在稀碱溶液中,连在苯环上的溴原子不易发生水解
②两个羟基同时连在同一碳原子上的结构是不稳定的,它将自动发生脱水反应:
CH3CH(OH) 2→CH3CHO +H2O
回答下列问题:
(1)X中官能团的名称是 ,C的结构简式为
(2)E→F反应类型是
(3)I的结构简式为 ;
(4)E不具有的化学性质 (选填序号)
a、取代反应 b、消去反应
c、氧化反应 d、1molE最多能与1mol NaHCO3反应
(5)写出下列反应的化学方程式:
①X与足量稀NaOH溶液共热的化学方程式:
②B→C的化学方程式: ;
(6)同时符合下列条件的E的同分异构体共有 种,
a、苯环上的一氯代物有两种 b、不能发生水解反应 c、遇FeCl3溶液不显色
d、1molE最多能分别与1molNaOH和2molNa反应
其中核磁共振氢谱为六组峰,且峰面积比为3:2:2:1:1:1的一种结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知:A为常见的短周期轻金属,含A的合金材料常用于火箭、飞机等制造业;B是一种盐,在工农业生产中用途较广;C、F、H为常见非金属单质;常温下C、F、I、E、J和K为气体;E对空气的相对密度为0.586;常温常压下G为液体。有关物质间的转化关系如下(图中部分反应物或产物已省略):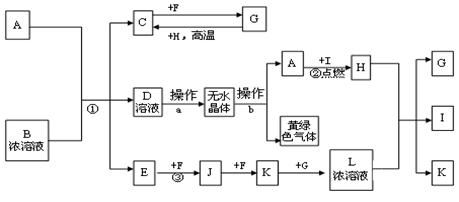
请填空:
(1)B的化学式为 。
(2)操作a必须在HCl气流中加热得无水物而不能直接加热浓缩,其原因是 ;操作b为 。
(3)反应①的离子反应方程式为 。反应③的化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。已知:碳酸不能溶解Al(OH)3沉淀。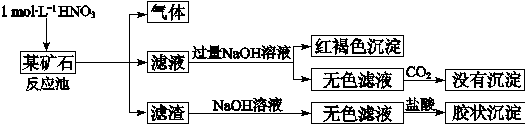
(1)Si在周期表中的位置是 。
(2)下列说法正确的是 。
a.酸性:H2CO3>H2SiO3
b.原子半径:O<C<Si<Al
c.稳定性:H2O>CH4>SiH4
d.离子半径:O2-<Al3+
(3)该矿石的组成是 ,滤渣和NaOH溶液反应的离子方程式是 。
(4)该矿石和1 mol L-1HNO3反应的离子方程式 。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,目的是 ;若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1 mol L-1 HNO3的体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
中学常见反应的化学方程式是:A+B→X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4。请回答:
(1)若Y是黄绿色气体,该反应的离子方程式是 。
(2)若A为常见的非金属单质,B的溶液为某浓酸,其氧化产物的结构式为 ______
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是 mol。
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
置换反应可用下图表示,回答下列问题:
(1)若甲为黄绿色气体,单质乙能使淀粉溶液变蓝色,则该反应的离子方程式为 。
(2)若过量单质甲与化合物A发生反应现象为溶液由蓝色变为浅绿色, 除去反应后混合物中剩余的甲所用的试剂名称是 写出单质甲与化合物A反就的离子方程式 。
(3)工业上利用置换反应原理制备一种半导体材料,写出该反应的化学方程式
(4)若单质乙是红色金属固体单质,化合物B常温下为无色液体,则该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,用化学用语回答下列问题:
Ⅰ.(1)请画出元素⑧的阴离子结构示意图 。
(2)④、⑤、⑦的原子半径由小到大的顺序为 。
(3)⑤和⑥的最高价氧化物对应水化物的碱性强弱为 > 。
(4)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为 。
Ⅱ.由表中①一⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答:
(1)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是 ;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式 。
(2)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为 ,写出A与C两溶液反应的离子方程式____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有A、B、C、D、E、F、G、H、I九种常见物质,它们的转化关系(反应条件未注明)如图所示。常温下A为液态,D为固态,B、C、E、G为气态(C可以使带火星木条复燃),其中B、C、D为单质,F为淡黄色粉末状化合物,I的焰色反应为黄色。
请回答:(1)写出F的电子式 。(2)G的结构式是 。
(3)反应④是 反应(填“吸热”或者“放热”)
(4)写出反应⑤的化学反应方程式
(5)B、C单质已被应用于字宙飞船的燃料电池中,如图所示。若将B换成甲烷也能组成燃料电池(两个电极均由多孔性碳构成),该电池工作时: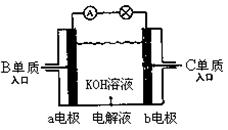
①b电极附近溶液的pH将 (填“增大”“减小”“不变”);
②a电极上的电极反应式为: 。
(6)在标准状况下,若将3.36L气体G通入50mL 4mol/L的H溶液中,用一个离子方程式表示其过程:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com