
ЈЁ10·ЦЈ©№ӨТөЦЖЗвЖшөДТ»ёцЦШТӘ·ҙУҰКЗЈәCO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
ЈЁ1Ј©ТСЦӘФЪ25ЎЈCКұЈә
ўЩ C(КҜД«)Ј«1/2O2(g)=CO(g) ЎчH1=Јӯ111kJЎӨmolЈӯ1
ўЪ C(КҜД«)Ј«O2(g)=CO2(g) ЎчH2=Јӯ394kJЎӨmolЈӯ1
ўЫ H2(g)Ј«1/2O2(g)=H2O(g) ЎчH3=Јӯ242kJЎӨmolЈӯ1
Фт·ҙУҰCO(g)+H2O(g) === CO2(g)+H2(g)өД·ҙУҰИИЎчH=___________.
ЈЁ2Ј©ПЦҪ«І»Н¬БҝөДCOЈЁgЈ©әНH2O(g)·ЦұрНЁИлөҪМе»эОӘ2LөДәгИЭГЬұХИЭЖчЦРҪшРР·ҙУҰЈ¬өГөҪИзПВИэЧйКэҫЭЈә

ўЩТФПВ·ҙУҰДЬЛөГчCO(g)+H2O(g)  CO2(g)+H2(g)ҙпөҪЖҪәвЧҙМ¬өДКЗ_________
CO2(g)+H2(g)ҙпөҪЖҪәвЧҙМ¬өДКЗ_________
AЈ®ИЭЖчЦРCOөДә¬БҝұЈіЦІ»ұд BЈ®ИЭЖчЦРCO2ЕЁ¶ИУлCOЕЁ¶ИПаөИ
CЈ® ЈЁCOЈ©=
ЈЁCOЈ©= (H2O) DЈ®ИЭЖчЦР»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝұЈіЦІ»ұд
(H2O) DЈ®ИЭЖчЦР»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝұЈіЦІ»ұд
ўЪКөСйIЦРЈ¬ҙУ·ҙУҰҝӘКјөҪ·ҙУҰҙпөҪЖҪәвКұЈ¬COөДЖҪҫщ·ҙУҰЛЩВК ЈЁCOЈ©=_____Ј»
ЈЁCOЈ©=_____Ј»
ўЫКөСйIIМхјюПВ·ҙУҰөДЖҪәвіЈКэK=_____________(ұЈБфРЎКэөгәу¶юО»)Ј»
ўЬКөСйIIIЦРЈ¬ИфЖҪәвКұЈ¬COөДЧӘ»ҜВКҙуУЪЛ®ХфЖшЈ¬ФтaЈ¬bұШРлВъЧгөД№ШПөКЗ______Ј»
ўЭИфФЪ900ЎжКұЈ¬КөСйII·ҙУҰҙпөҪЖҪәвәуЈ¬ПтҙЛИЭЖчЦРФЩјУИл1molCOЎў0.5mol H2OЎў0.2mol CO2Ўў0.5mol H2Ј¬ФтҙЛКұ ___________
___________ (МоЎ°>Ўұ»тЎ°<Ўұ)Ј¬ЖҪәвПт__________·ҪПтТЖ¶ҜЈЁМоЎ°Хэ·ҙУҰЎұЎўЎ°Дж·ҙУҰЎұЎ°І»ТЖ¶ҜЎұЈ©
(МоЎ°>Ўұ»тЎ°<Ўұ)Ј¬ЖҪәвПт__________·ҪПтТЖ¶ҜЈЁМоЎ°Хэ·ҙУҰЎұЎўЎ°Дж·ҙУҰЎұЎ°І»ТЖ¶ҜЎұЈ©
ЈЁ1Ј©-41kJЎӨmolЈӯ1ЈЁ2·ЦЈ©ЈЁ2Ј©ўЩAЈЁ1·ЦЈ© ўЪ0.16molЎӨLЈӯ1ЎӨminЈӯ1 ЈЁ2·ЦЈ©
ўЫ0.33ЈЁ2·ЦЈ© ўЬa<b(1·Ц) ўЭ> Хэ·ҙУҰЈЁёч1·ЦЈ©
ЎҫҪвОцЎҝ
КФМв·ЦОцЈәЈЁ1Ј©ўЪЈӯўЩЈӯўЫЈ¬ХыАнҝЙөГЈәCO(g)+H2O(g) == CO2(g)+H2(g)ЎчH=-41kJ/molЈ»ЈЁ2Ј©ўЩA.ИфИЭЖчЦРCOөДә¬БҝұЈіЦІ»ұдЈ¬ФтЖдЕЁ¶ИІ»ұдЈ¬·ҙУҰҙҰУЪЖҪәвЧҙМ¬Ј¬ХэИ·Ј» BЈ®ИЭЖчЦРCO2ЕЁ¶ИУлCOЕЁ¶ИПаөИЈ¬·ҙУҰҝЙДЬҙҰУЪЖҪәвЧҙМ¬Ј¬ТІҝЙДЬҙҰУЪ·ЗЖҪәвЧҙМ¬Ј¬ТтҙЛІ»ДЬЧчОӘЕР¶П·ҙУҰҙҰУЪЖҪәвЧҙМ¬өДұкЦҫЈ¬ҙнОуЈ» CЈ®ОЮВЫ·ҙУҰКЗ·сҙпөҪЖҪәвЈ¬¶јҙжФЪV(Хэ)ЈЁCOЈ©= V(Хэ) (H2O) Ј¬ЛщТФІ»ДЬЕР¶П·ҙУҰҙҰУЪЖҪәвЧҙМ¬Ј¬ҙнОуЈ» DЈ®УЙУЪИЭЖчөДИЭ»эІ»ұдЈ¬ЖшМеөДОпЦКөДБҝІ»ұдЈ¬ЛщТФОЮВЫ·ҙУҰҪшРРөҪИОәОіМ¶ИЈ¬ИЭЖчЦР»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝ¶јІ»ұдЈ¬ТтҙЛІ»ДЬЕР¶П·ҙУҰҙҰУЪЖҪәвЧҙМ¬Ј¬ҙнОуЈ»ўЪКөСйIЦРЈ¬ҙУ·ҙУҰҝӘКјөҪ·ҙУҰҙпөҪЖҪәвКұЈ¬COөДЖҪҫщ·ҙУҰЛЩВКVЈЁCOЈ©=(1.6molЎВ2L)ЎВ5min=0.16mol/(LЎӨmin)Ј» ўЫКөСйIIМхјюПВ·ҙУҰөДЖҪәвіЈКэK=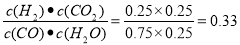 Ј»ўЬУЙУЪФЪЖдЛьМхјюІ»ұдКұЎЈФцҙу·ҙУҰОпөДЕЁ¶ИҝЙТФКЗЖдЛь·ҙУҰОпөДЧӘ»ҜВКМбёЯЈ¬¶шЖдұҫЙнөДЧӘ»ҜВКҪөөНЈ¬ЛщТФФЪКөСйIIIЦРЈ¬ИфЖҪәвКұЈ¬COөДЧӘ»ҜВКҙуУЪЛ®ХфЖшЈ¬ФтaЈ¬bұШРлВъЧгөД№ШПөКЗ¶юХЯөДОпЦКөДБҝөДұИРЎУЪ·ҪіМКҪЦРөДјЖБҝ№ШПөөДұИЈ¬јҙa<bЈ»ўЭИфФЪ900ЎжКұЈ¬КөСйII·ҙУҰҙпөҪЖҪәвәуЈ¬ПтҙЛИЭЖчЦРФЩјУИл1molCOЎў0.5mol H2OЎў0.2mol CO2Ўў0.5mol H2Ј¬ФтҙЛКұУЙУЪQ=
Ј»ўЬУЙУЪФЪЖдЛьМхјюІ»ұдКұЎЈФцҙу·ҙУҰОпөДЕЁ¶ИҝЙТФКЗЖдЛь·ҙУҰОпөДЧӘ»ҜВКМбёЯЈ¬¶шЖдұҫЙнөДЧӘ»ҜВКҪөөНЈ¬ЛщТФФЪКөСйIIIЦРЈ¬ИфЖҪәвКұЈ¬COөДЧӘ»ҜВКҙуУЪЛ®ХфЖшЈ¬ФтaЈ¬bұШРлВъЧгөД№ШПөКЗ¶юХЯөДОпЦКөДБҝөДұИРЎУЪ·ҪіМКҪЦРөДјЖБҝ№ШПөөДұИЈ¬јҙa<bЈ»ўЭИфФЪ900ЎжКұЈ¬КөСйII·ҙУҰҙпөҪЖҪәвәуЈ¬ПтҙЛИЭЖчЦРФЩјУИл1molCOЎў0.5mol H2OЎў0.2mol CO2Ўў0.5mol H2Ј¬ФтҙЛКұУЙУЪQ=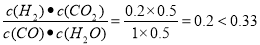 Ј¬ЛщТФ
Ј¬ЛщТФ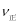 >
>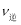 (МоЎ°Ўұ»тЎ°<Ўұ)Ј¬ЖҪәвПтПтХэ·ҙУҰ·ҪПтТЖ¶ҜЎЈ
(МоЎ°Ўұ»тЎ°<Ўұ)Ј¬ЖҪәвПтПтХэ·ҙУҰ·ҪПтТЖ¶ҜЎЈ
ҝјөгЈәҝјІйИИ»ҜС§·ҪіМКҪөДКйРҙЎўҝЙДж·ҙУҰЖҪәвЧҙМ¬өДЕР¶ПЎў»ҜС§·ҙУҰЛЩВКЎў»ҜС§ЖҪәвІъЙъөДјЖЛгЎўОпЦКЧӘ»ҜВКөДҙуРЎұИҪПәНУ°ПмТтЛШЎў»ҜС§·ҙУҰҪшРРөД·ҪПтөДЕР¶ПөДЦӘК¶ЎЈ


 РЎС§КэС§ҝЪЛгМвҝЁНСҝЪ¶шіцПөБРҙр°ё
РЎС§КэС§ҝЪЛгМвҝЁНСҝЪ¶шіцПөБРҙр°ё УЕРгЙъУҰУГМвҝЁҝЪЛгМмМмБ·ПөБРҙр°ё
УЕРгЙъУҰУГМвҝЁҝЪЛгМмМмБ·ПөБРҙр°ё ХгҪӯЦ®РЗҝОКұУЕ»ҜЧчТөПөБРҙр°ё
ХгҪӯЦ®РЗҝОКұУЕ»ҜЧчТөПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015ҪмБЙДюКЎ·ЦРЈёЯИэЙПС§ЖЪЖЪіхҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
(6·Ц)ВИ»ҜНӯҫ§Ме(CuCl2ЎӨ2H2O)ә¬УРFeCl2ФУЦКЈ¬ОӘЦЖөГҙҝҫ»ВИ»ҜНӯҫ§МеЈ¬КЧПИҪ«ЖдЦЖіЙЛ®ИЬТәЈ¬И»әу°ҙПВБРІЩЧчІҪЦиҪшРРМбҙҝЈә
ўЩПИјУИлСх»ҜјБXЈ¬ФЩјУИлОпЦКYЈ¬№эВЛөГіБөнZЈ»
ўЪҪ«ВЛТәХф·ўҪбҫ§өГҙҝCuCl2ЎӨ2H2Oҫ§МеЎЈ
ТСЦӘЈәИэЦЦАлЧУҙУИЬТәЦРНкИ«іКЗвСх»ҜОпіБөнЛщРиpHЦөЈәFe3+Јә3Ј®7Ј¬Cu2+Јә6Ј®4Ј¬Fe2+Јә6Ј®4КФ»ШҙрПВБРОКМвЈә
ЈЁ1Ј©јУИлСх»ҜјБXөДФӯТтКЗ____ __ЎЈ
ЈЁ2Ј©ПВБРОпЦК¶јҝЙТФЧчОӘСх»ҜјБЈ¬ЖдЦРЧоККТЛУЪұҫКөСйөДКЗЈЁ Ј©
AЈ®H2O2 BЈ®KMnO4 CЈ®NaClO DЈ®K2CrO7
ЈЁ3Ј©ОпЦКYКЗ__ ____Ј¬іБөнZКЗ__ ____Ј®
ЈЁ4Ј©ОӘ·ЦАліціБөнZЈ¬ІЙИЎөДКөСйІЩЧчЛщУГТЗЖчУР__ ____ЎЈ
ЈЁ5Ј©ІЩЧчўЪЛщУГөДТЗЖчУР____ __ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015ҪмБЙДюЙтСфКРёЯИэЙПС§ЖЪөЪТ»ҙОДЈДвҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ClO2КЗТ»ЦЦПы¶ҫЙұҫъР§ВКёЯЎў¶юҙООЫИҫРЎөДЛ®ҙҰАнјБЎЈКөСйКТҝЙНЁ№эТФПВ·ҙУҰЦЖөГClO2Јә2KClO3+H2C2O4+H2SO4  2ClO2Ўь+2CO2Ўь+K2SO4+2H2OЎЈПВБРЛө·ЁХэИ·өДКЗ
2ClO2Ўь+2CO2Ўь+K2SO4+2H2OЎЈПВБРЛө·ЁХэИ·өДКЗ
AЈ®H2SO4КЗСх»ҜјБ BЈ®ClO2КЗСх»ҜІъОп
CЈ®H2C2O4ФЪ·ҙУҰЦРұ»Сх»Ҝ DЈ®1 molKClO3ІОјУ·ҙУҰУР2molөзЧУЧӘТЖ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015ҪмБЙДюЙтСфКРёЯИэЙПС§ЖЪөЪТ»ҙОДЈДвҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРОпЦКөДК№УГІ»Йжј°»ҜС§ұд»ҜөДКЗ
AЈ®Гч·ҜУГЧчҫ»Л®јБ BЈ®Тә°ұУГЧчЦЖАдјБ CЈ®Зв·ъЛбҝМКҙІЈБ§ DЈ®ЙъКҜ»ТЧчёЙФпјБ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015Ҫм№уЦЭКЎ№уСфКРёЯИэДкј¶8ФВГюөЧҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәМоҝХМв
ЈЁ6·ЦЈ©МјКЗРОіЙ»ҜәПОпЦЦАаЧо¶аөДФӘЛШЎЈ
ЈЁ1Ј©CH2=CH-CЎФNКЗЦЖұёлжВЪөДФӯБПЈ¬Жд·ЦЧУЦР јьәН
јьәН јьөДёцКэЦ®ұИОӘ__________(МоЧојтХыКэұИ)Ј»
јьөДёцКэЦ®ұИОӘ__________(МоЧојтХыКэұИ)Ј»
ЈЁ2Ј©ТТҙјCH3CH2OHУлјЧГСCH3OCH3өД·ЦЧУКҪҫщОӘC2H6OЈ¬ө«CH3CH2OHөД·РөгёЯУЪCH3OCH3өД·РөгЈ¬ЖдФӯТтКЗ____________________Ј»
ЈЁ3Ј©ДіФӘЛШО»УЪөЪ4ЦЬЖЪVIIЧеЈ¬Жд»щМ¬ФӯЧУөДОҙіЙ¶ФөзЧУКэУл»щМ¬МјФӯЧУөДОҙіЙ¶ФөзЧУКэПаН¬Ј¬ФтЖд»щМ¬ФӯЧУөДјЫІгөзЧУЕЕІјКҪОӘ_______________.
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015Ҫм№уЦЭКЎ№уСфКРёЯИэДкј¶8ФВГюөЧҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРУГУЪҪвКНКөСйКВКөөД»ҜС§·ҪіМКҪХэИ·өДКЗЈЁ Ј©
AЈ®Al2(SO4)3ИЬТәөОјУ°ұЛ®ІъЙъ°ЧЙ«ҪәЧҙіБөнЈәAl3++3OH-= Al(OH)3 
BЈ®ҙҝјоИЬТәК№·УМӘұдәмЈәCO32-+2H2O ?H2CO3+2OH-
CЈ®ТТЛбЗеіэЛ®№ёәуөД»ҜС§·ҙУҰФӯАнЈә2H++CO32-= CO2 + H2O
+ H2O
DЈ®FeCl3ИЬТәЦРјУИлЧгБҝМъ·ЫЈ¬ИЬТәУЙ»ЖЙ«ұдіЙЗіВМЙ«Јә2Fe3++ Fe=3Fe2+
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015Ҫм№уЦЭКЎ№уСфКРёЯИэДкј¶8ФВГюөЧҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБР№ШУЪCЎўSiЎўGeЎўSnЎўPbөДұИҪПЈ¬ХэИ·өДКЗЈЁ Ј©
AЈ®ЛьГЗөДЧоНвІгөзЧУКэЛжәЛөзәЙКэФцјУ¶шФц¶а
BЈ®ЛьГЗөДЧоёЯјЫСх»ҜОпҫщҝЙИЬУЪЛ®ЙъіЙПаУҰөДЛб
CЈ®ЛьГЗөҘЦКөДСх»ҜРФЛжәЛөзәЙКэөДФцјУ¶шЦрҪҘјхИх
DЈ®ЛьГЗөДЗв»ҜОпөДОИ¶ЁРФЛжәЛөзәЙКэөДФцјУ¶шЦрҪҘФцЗҝ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015ҪмёЈҪЁКЎёЯ¶юЙПС§ЖЪөЪ¶юҙОФВҝј»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
25ЎжКұЈ¬Л®өДөзАлҙпөҪЖҪәвЈәH2O  HЈ«Ј«OHЎӘ ҰӨHЈҫ0Ј¬ПВБРРрКцХэИ·өДКЗЈЁ Ј©
HЈ«Ј«OHЎӘ ҰӨHЈҫ0Ј¬ПВБРРрКцХэИ·өДКЗЈЁ Ј©
AЈ®ПтЛ®ЦРјУИлЗвСх»ҜДЖЈ¬ЖҪәвДжПтТЖ¶ҜЈ¬c(HЈ«)ҪөөНЈ¬c(OHЁD)Фцҙу
BЈ®ПтЛ®ЦРјУИлЙЩБҝ№ММеБтЛбЗвДЖЈ¬c(HЈ«)ФцҙуЈ¬Kwұдҙу
CЈ®ПтЛ®ЦРјУИлЙЩБҝ№ММеCH3COOHЈ¬ЖҪәвДжПтТЖ¶ҜЈ¬c(HЈ«)ҪөөН
DЈ®Ҫ«Л®јУИИЈ¬KwФцҙуЈ¬c(HЈ«)І»ұд
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә2015ҪмёЈҪЁКЎёЯИэЙПС§ЖЪЖЪЦРҝјКФ»ҜС§КФҫнЈЁҪвОц°жЈ© МвРНЈәСЎФсМв
ПВБРРрКцХэИ·өДКЗ
AЈ®48g O3ЖшМеә¬УР6.02ЎБ1023ёцO3·ЦЧУ
BЈ®5.6g FeУлЧгБҝөДПЎСОЛб·ҙУҰЧӘТЖөзЧУ0.3 mol
CЈ®0.5molЎӨL-1CuCl2ИЬТәЦРә¬УР3.01ЎБ1023ёцCu2+
DЈ®ұкЧјЧҙҝцПВЈ¬33.6LH2Oә¬УР9.03ЎБ1023ёцH2O·ЦЧУ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com