
| 7 |
| 14 |
| 16 |
| 16 |


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
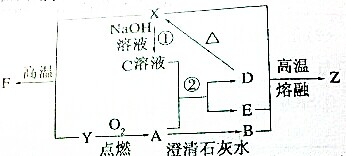 已知下列物质有如图所示转化关系,水和部分产物已略去.
已知下列物质有如图所示转化关系,水和部分产物已略去.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入水时,平衡向逆反应方向移动 |
| B、加入少量NaOH固体,平衡向正反应方向移动 |
| C、通入少量HCl气体,溶液中PH值增大 |
| D、加入少量CH3COONa固体,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
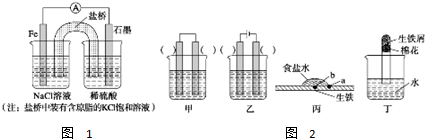
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、H2C2O4在反应中被氧化 |
| B、KClO3在反应中得到电子 |
| C、CO2是还原产物 |
| D、4 molKClO3参加反应有8 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
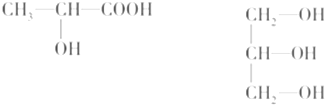
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纳米材料直径一般在几纳米到几十纳米(1nm=10-9m)之间,因此纳米材料属于胶体 |
| B、青铜是我国使用最早的合金 |
| C、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| D、明矾与漂白粉都是水处理药品,原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、红热的铜丝在氯气中剧烈燃烧,生成棕黄色烟 |
| B、钠在氯气中燃烧,生成白色的烟 |
| C、纯净的氢气在氯气中安静的燃烧,在集气瓶口形成白色烟雾 |
| D、氯气能与水反应生成盐酸和次氯酸,次氯酸见光易分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com