
分析 (1)HCl水溶液溶液中完全电离,CH3COOH部分电离,水电离出的氢离子浓度和电离出的氢氧根离子浓度相同,结合溶液中离子积常数分析判断;
(2)碳酸钠中碳酸根离子水解程度大于碳酸氢根离子.
解答 解:(1)HCl水溶液溶液中完全电离,CH3COOH部分电离,等物质的量浓度的溶液中,HCl完全电离,氢离子浓度大,对水电离的抑制程度大,水电离出的氢离子浓度和电离出的氢氧根离子浓度相同,HCl溶液中水电离出的c水(H+)=c水(OH-)小,所以水电离出的c(H+):HCl<CH3COOH,
故答案为:<;
(2)碳酸钠中碳酸根离子水解程度大于碳酸氢根离子,pH相同的溶液中:c(Na2CO3)<c(NaHCO3),
故答案为:<.
点评 本题考查了水溶液中离子水解分析判断,影响水电离平衡因素分析,盐类水解的理解应用是解题关键,题目较简单.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 基态原子核外三个能级有电子,且每个能级上电子数目相同 |
| B | 其一种单质被称为地球生物的“保护伞” |
| C | 单质为常见金属,离子半径在同周期中最小 |
| D | 基态原子最外层电子排布为(n+1)sn(n+1)p(n+2) |
| E | 有多种化合价,有一种氧化物为黑色磁性晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用澄清石灰水可区别Na2CO3和NaHCO3粉末 | |
| B. |  用如图装置进行浓硝酸与铜的反应制取并收集NO2 用如图装置进行浓硝酸与铜的反应制取并收集NO2 | |
| C. | 检验未知溶液是否含SO42ˉ可先加氯化钡,再加稀盐酸 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,可依次加入H2O、NaOH、BaCl2、Na2CO3,过滤再加入HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
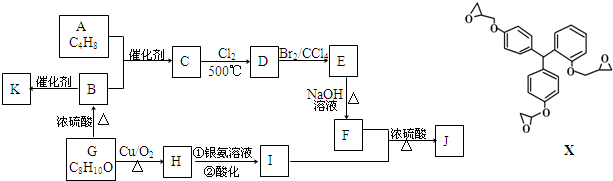
 .
.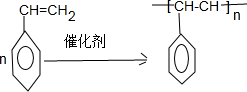 ;F+I→J
;F+I→J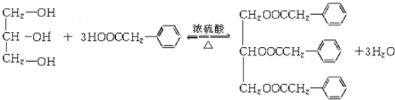 .
. (其中三种).
(其中三种).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
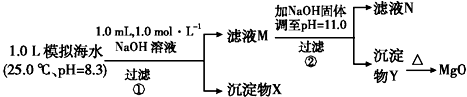
| 模拟海水中的离 子浓度/mol•L-1 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
| A. | 沉淀物X为CaCO3、MgCO3 | |
| B. | 滤液M中存在Mg2+,Ca2+ | |
| C. | 滤液N中存在Ca2+,没有Mg2+ | |
| D. | 步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为仍Mg(OH)2,没有Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子晶体 | 原子晶体 | 分子晶体 | |
| A | NaOH | Ar | SO2 |
| B | H2SO4 | 石墨 | S |
| C | CH3COONa | 水晶 | CH3CH3 |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com