
某次实验需用0.4 mol/L NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_______________mL容量瓶;
(2)用托盘天平准确称量__________g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待__________________后,将烧杯中的溶液注入容量瓶中;用少量蒸馏水洗涤烧杯 次,洗涤后的溶液一并转入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;向容量瓶中加入蒸馏水,到液面_____________________时,改用__________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均匀;若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是___________,偏低的是___________,对实验结果没有影响的是___________(填各选项的序号)。
| A.所用的NaOH中混有少量Na2O |
| B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥 |
| C.配制溶液所用的容量瓶洗净后没有烘干 |
| D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 |
(1)500
(2)8.0
(3)待冷却至室温后后
(4)2-3 次
(5)离刻度线1~2cm时 胶头滴管
(6)偏高的是ADF 偏低的是EG 没有影响的是BC
解析试题分析:(1)因溶液的体积480mL,但容量瓶的规格没有480mL,所以选用500mL容量瓶,故答案为:500mL;
(2)需氢氧化钠的质量为m=0.5L×0.4mol?L-1×40g/mol=8.0g,故答案为:8.0;
(3)氢氧化钠溶解放出大量的热,溶液具有热胀冷缩的性质,影响溶液体积,故应先冷却至室温,故答案为:待溶液冷却至室温;
(4)为保证溶质尽可能转移到容量瓶中,需用少量蒸馏水洗涤烧杯2-3 次,并将洗涤液一起转入容量瓶中,故答案为:蒸馏水;一起转入容量瓶中;
(5)向容量瓶中加入蒸馏水,到液面离刻度线1-2cm时,改用胶头滴管加蒸馏水至液面最低点与刻度线相切.盖好瓶塞,上下颠倒混合均匀,故答案为:1~2cm;胶头滴管;上下颠倒混合均匀;
(6) A设NaOH和Na2O的质量相同为m,则NaOH的物质的量为m/40,Na+的物质的量为m/40。 Na2O的物质的量为m/52 ,Na+的物质的量为m/31。所以NaOH中混有少量Na2O会导致溶液浓度增大;B、C最后需要定容,容量瓶洗净后没有烘干,对溶液浓度无影响;D氢氧化钠溶解放出大量的热,溶液具有热胀冷缩的性质,故应先冷却至室温再移液定容,所以固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶后,进行后面的操作会使得溶液的体积变小,所以溶液浓度偏高;E转移溶液后,未洗涤烧杯和玻璃棒就直接定容,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低;F定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏高。 G.定容摇匀后静止,液面会低于刻度线,因为会有一部分溶液挂在容器壁上,如向此溶液中加蒸馏水,会将溶液稀释。
考点:配制一定物质的量浓度的溶液


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:计算题
6.5g锌和100mL2mol/L稀硫酸完全反应,反应后溶液的体积仍为100mL。求:
(1)在标准状况下,生成气体的体积;
(2)生成物的物质的量浓度;
(3)反应后的溶液中SO 的物质的量浓度;
的物质的量浓度;
(4)在反应后的溶液中加入1mol/L氢氧化钾溶液,恰好使其中的金属离子完全沉淀时,需加入氢氧化钾溶液的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的物质的量浓度。
(1)在容量瓶的使用方法中,下列操作不正确的是(填字母)________。
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液润洗 |
| C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
| D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(1)容量瓶上含有下列量中的(填写字母)
A、压强 B、温度 C、容积 D、密度 E、刻度线
(2)用浓硫酸配制250mL2mol?L-1硫酸溶液时,所需的玻璃仪器除烧杯、玻璃棒和胶头滴管之外,还需要 (填仪器名称);在下列配制过程示意图中,有错误的是(填写序号) 。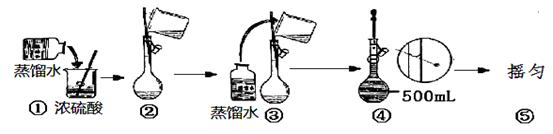
(3)现要用容量瓶配制500mL0.4mol?L-1Na2CO3溶液,配好的溶液倒入试剂瓶后需要贴上标签。请你帮助把下图标签上的内容填上去。
(4)下列情况将使配制溶液的物质的量浓度偏低的有 (填序号)
A.容量瓶用蒸馏水洗净后,未待干燥便用来配制
B.NaOH溶解后趁热移入容量瓶中
C.定容时,俯视刻度线
D.摇匀后发现液面未到刻度线,继续加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室需要0.1mol/LNaOH溶液450mL 和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 ______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。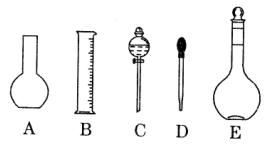
(2)下列操作中,容量瓶所不具备的功能有_________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为__________g。配制时,其正确的操作顺序是字母表示,
每个字母只能用一次)____________。
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)根据计算得知,所需质量分数为98%、密度为1.84g/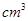 的浓硫酸的体积为:__________mL(计算
的浓硫酸的体积为:__________mL(计算
结果保留一位小数)。如果实验室有15mL、20mL、50mL量筒,应选用____________mL的量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于一些重要的化学概念有下列说法:①Fe(OH)3胶体和CuSO4溶液都是混合物;②BaSO4是一种难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④煤的干馏、煤的汽化和液化都属于化学变化;⑤置换反应都属于离子反应。其中正确的是( )
| A.①②⑤ | B.①②④ | C.②③④ | D.③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法不正确的是
| A.胶体的分散质粒子直径大小介于溶液与浊液之间 |
| B.金属冶炼通常利用氧化还原反应原理 |
| C.陶瓷、水泥和光导纤维均属于硅酸盐材料 |
| D.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.单质铯的熔点比单质锂的高 |
| B.胶体的胶粒不能通过滤纸 |
| C.元素N的氢化物的沸点比元素P的氢化物的沸点低 |
| D.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
| A.NO2溶于水得到HNO3,所以NO2属于酸性氧化物 |
B.过氧化钠与水反应的离子方程式为: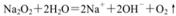 |
| C.漂白粉和水玻璃长期暴露在空气中失效,其原理完全相同 |
| D.足量Zn与一定量浓硫酸充分反应得到混合气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com