
【题目】在容积为2 L的恒容密闭容器中充入1 mol CO2(g)和3.5 mol H2(g),在一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol。该反应的平衡常数K与温度T的关系如图1所示,CO2的转化率如图2所示,下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol。该反应的平衡常数K与温度T的关系如图1所示,CO2的转化率如图2所示,下列说法错误的是

A. 在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系
B. 该温度下,平衡常数K=0.25
C. 其他条件不变下,图2中x可表示温度或压强或投料比c(CO2)/c(H2)
D. 用二氧化碳合成甲醇体现了碳减排理念
【答案】C
【解析】
在容积为2 L的恒容密闭容器中充入1 mol CO2(g)和3.5 mol H2(g),在一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol,
CH3OH(g)+H2O(g) ΔH<0。反应进行8 min时达到平衡状态,测得n(CH3OH)=0.5mol,
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始(mol) 1 3.5 0 0
反应(mol) 0.5 1.5 0.5 0.5
平衡(mol) 0.5 2 0.5 0.5
据此分析解答。
A.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0,为放热反应,升高温度,平衡逆向移动,平衡常数K减小,因此在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系,故A正确;
CH3OH(g)+H2O(g) ΔH<0,为放热反应,升高温度,平衡逆向移动,平衡常数K减小,因此在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系,故A正确;
B.根据上述分析,该温度下,平衡常数K=![]() =
=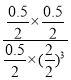 = 0.25,故B正确;
= 0.25,故B正确;
C.根据CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0,温度升高,平衡逆向移动,二氧化碳的转化率降低,与图像相符;压强增大,平衡正向移动,二氧化碳的转化率增大,与图像不符;投料比c(CO2)/c(H2)增大,二氧化碳的转化率减小,与图像相符;因此图2中x不可以表示压强,故C错误;
CH3OH(g)+H2O(g) ΔH<0,温度升高,平衡逆向移动,二氧化碳的转化率降低,与图像相符;压强增大,平衡正向移动,二氧化碳的转化率增大,与图像不符;投料比c(CO2)/c(H2)增大,二氧化碳的转化率减小,与图像相符;因此图2中x不可以表示压强,故C错误;
D.用二氧化碳合成甲醇,能够减少二氧化碳的排放量,体现了碳减排理念,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】(1)有BaCl2和KCl的混合溶液V L,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀,消耗a mol H2SO4;另一份滴加AgNO3溶液,消耗b mol AgNO3使Cl-完全沉淀。原混合溶液中的K+的物质的量浓度为___mol·L-1。
(2)一定条件下,PbO2与Cr3+反应,产物是![]() 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为____mol;
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为____mol;
(3)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子数之比为___________。
(4)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。Al+NO3-+ —AlO2-+N2↑+H2O,_____________
(5)某化学反应的反应物和产物:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
①该反应的氧化产物是__________。
②若该反应方程式中I2和KIO3的计量数分别是是6和3,请在下边的化学式上用单线桥标出电子转移的方向和数目:KMnO4+KI+H2SO4→__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
C.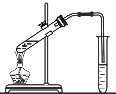 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 石灰岩受地下水长期溶蚀形成溶洞
石灰岩受地下水长期溶蚀形成溶洞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构的叙述不正确的是( )
A.一氟一氯甲烷只有一种结构,可以证明甲烷是正四面体结构
B.构成乙烯分子的所有原子都在同一平面内,其分子中只含有极性键
C.邻二甲苯没有同分异构体表明苯的凯库勒结构式不准确
D.![]() 和CH3一CH=CH2互为同分异构体
和CH3一CH=CH2互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂钒氧化物电池的能量密度远远超过其他材料电池,其成本低,便于大量推广,且对环境无污染。已知电池的总反应为V2O5+xLi![]() LixV2O5,下列说法正确的是
LixV2O5,下列说法正确的是
A. 电池在放电时,Li+向电源负极移动
B. 充电时阳极的反应为LixV2O5-xe-===V2O5+xLi+
C. 放电时负极失重7.0 g,则转移2 mol电子
D. 该电池以Li、V2O5为电极,酸性溶液作介质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________。
(2)丙溶液中存在的电离平衡为______________(用电离平衡方程式表示)。
(3)常温下,用水稀释0.1 mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是________(填序号)。
①n(H+) ②c(H+) ③ c(CH3COOH)/c(CH3COO-) ④c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为___________。
(5)某同学用甲溶液分别滴定20.00 mL乙溶液和20.00 mL丙溶液,得到如图所示的两条滴定曲线,请回答有关问题:
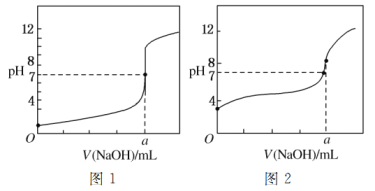
①甲溶液滴定丙溶液的曲线是________(填“图1”或“图2”)曲线。
②a=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_____;Ti原子核外共有________种运动状态不同的电子。
(2)BH3分子与NH3分子的空间结构分别为_________;BH3与NH3反应生成的BH3·NH3分子中含有的化学键类型有_______,在BH3·NH3中B原子的杂化方式为________。
(3)N和P同主族。科学家目前合成了N4分子,该分子中N—N—N键的键角为________;N4分解后能产生N2并释放出大量能量,推测其用途___________。(写出一种即可)
(4)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是____。
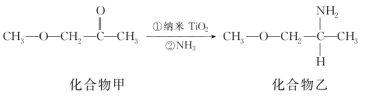
(5)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图所示。化合物乙的沸点明显高于化合物甲,主要原因是______。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。
(1)电石水化法制乙炔是将生石灰与焦炭在3000℃下反应生成CaC2,CaC2再与水反应即得到乙炔。CaC2与水反应的化学方程式为____
(2)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(1) △H1=-890.3kJ/mol
C2H2(g)+2.50(g)===2CO2(g)+H2O(1) △H2=-1299.6J/mol
2H2(g)+O2(g)=2H2O(1) △H3=-571.6kJ/mol
则甲烷气相裂解反应:2CH4(g)===C2H2(g)+3H2(g)的△H=_____kJ/mol。
(3)哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。
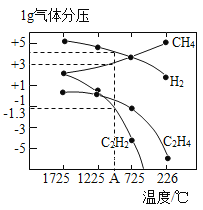
①T1℃时,向1L恒容密闭容器中充入0.3 mol CH4只发生反应2CH4(g)![]() C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=c(CH4)。该反应的△H____0(填“>”或“<”),CH4的平衡转化率为____%(保留3位有效数字)。上述平衡状态某一时刻,若改变温度至T2℃,CH4以0.01mol/(L·s)的平均速率增多,经ts后再次达到平衡,平衡时,c(CH4)=2c(C2H4),则T1_____(填“>”或“<”)T2,t=______s。
C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=c(CH4)。该反应的△H____0(填“>”或“<”),CH4的平衡转化率为____%(保留3位有效数字)。上述平衡状态某一时刻,若改变温度至T2℃,CH4以0.01mol/(L·s)的平均速率增多,经ts后再次达到平衡,平衡时,c(CH4)=2c(C2H4),则T1_____(填“>”或“<”)T2,t=______s。
②列式计算反应2CH4(g)![]() C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=____(用平衡分压代替平衡浓度计算,lg0.05=-1.3)。
C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=____(用平衡分压代替平衡浓度计算,lg0.05=-1.3)。
③由图可知,甲烷裂解制乙炔有副产物乙烯生成,为提高甲烷制乙炔的转化率,除改变温度外,还可采取的措施有___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的结构简式如图所示。则下列有关说法中不正确的是
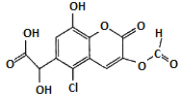
A. 能发生加成、取代、氧化反应B. 能与FeC13溶液发生显色反应
C. 1mol该物质最多可与6molH2反应D. 1mol该物质最多可与7molNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com