解答:
解:(1)明矾含有铝离子和钾离子两种阳离子,属于复盐,所以明矾是强电解质,在溶液中完全电离出钾离子、铝离子和硫酸根离子,电离方程式为:KAl(SO
4)
2?12H
2O=K
++Al
3++2SO
42-+12H
2O,
故答案为:KAl(SO
4)
2?12H
2O=K
++Al
3++2SO
42-+12H
2O;
(2)明矾的相对分子质量为474,23.7g明矾的物质的量为:n=
=
=0.05mol,明矾的电离方程式为:KAl(SO
4)
2?12H
2O=K
++Al
3++2SO
42-+12H
2O,所以所含的K
+和SO
42-的物质的量之比为0.05mol:2×0.05mol=1:2,n(H
2O)=12×0.05mol=0.6mol,m(H
2O)=nM=0.6mol×18 g/mol=10.8,
故答案为:1:2;10.8g;
(3)1.204×10
23个水分子,n(H
2O)=
=
=0.2mol,明矾的电离方程式为:KAl(SO
4)
2?12H
2O=K
++Al
3++2SO
42-+12H
2O,所以n[KAl(SO
4)
2?12H
2O]=
×0.2mol=
mol,m[KAl(SO
4)
2?12H
2O]=nM=
×474g/mol=7.9g,
故答案为:7.9g.



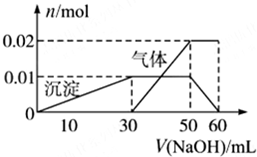 某无色溶液中含有NH4+、K+、Al3+、SO42-四种离子,进行如下实验:
某无色溶液中含有NH4+、K+、Al3+、SO42-四种离子,进行如下实验: