
已知某主族金属元素X的原子核内质子数和中子数之比为1∶1,含该金属阳离子0.192g的溶液恰好能将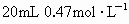 的
的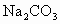 溶液中的
溶液中的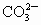 全部沉淀,推断X是什么元素及在周期表中的位置.
全部沉淀,推断X是什么元素及在周期表中的位置.
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
已知某主族金属元素X的原子核内质子数和中子数之比为1∶1,含该金属阳离子0.192g的溶液恰好能将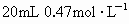 的
的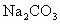 溶液中的
溶液中的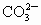 全部沉淀,推断X是什么元素及在周期表中的位置.
全部沉淀,推断X是什么元素及在周期表中的位置.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某主族金属元素X的原子核内质子数和中子数之比为1:1,含该金属阳离子0.192g的溶液恰好能将20mL0.4mol/L的Na2CO3溶液中的CO32-全部沉淀,推断X是什么元素及在周期表中的位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某主族金属元素X的原子核内质子数和中子数之比为1:1,含该金属阳离子0.192g的溶液恰好能将20mL0.4mol/L的Na2CO3溶液中的CO32-全部沉淀,下列推断正确的是X为镁,位于周期表第3周期,第ⅡA族
A、X为钙 B、X位于周期表第3周期
C、X位于周期表第2周期 D、X位于第ⅡA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com