
| A、CO2 |
| B、CaCl2 |
| C、NaOH |
| D、HCl |


科目:高中化学 来源: 题型:
| A、X的能量一定高于M的能量 |
| B、该反应是吸热反应,所以一定需要加热才能进行 |
| C、断裂反应物中化学键吸收的能量小于形成生成物中化学键放出的能量 |
| D、X和Y的总能量低于M和N的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中不可能存在非极性键 |
| B、不同非金属元素原子之间形成的化学键都是极性键 |
| C、极性键形成的一定是极性分子 |
| D、非极性分子中不可能既含极性键又含非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z是酸酐,但它不和水反应 |
| B、Z是一种碱性氧化物 |
| C、Z的化学式可能为X2Y5 |
| D、Z熔化时破坏化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素Y的最高化合价为+7 |
| B、三种元素的原子半径:X>Y>Z |
| C、Z的非金属性比Y的非金属性强 |
| D、化合物X2Z2中阴阳离子数之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
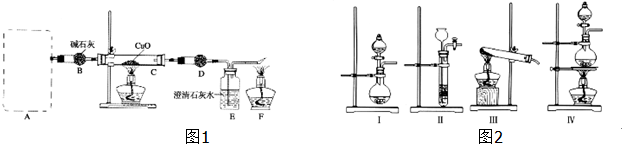
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com