
�������ӷ�Ӧ����ʽ��ȷ����
A����̼����þ��Һ�м�������Ca(OH)2��Һ��
Mg2+��HCO3����Ca2+��2OH�C== MgCO3����CaCO3����2H2O
B����̼������Һͨ������Ķ�����̼���壺CO32-��CO2��H2O��2HCO3��
C�����Ȼ�������Һ��ϡ�����ϣ�3Fe2++ 4H++NO3-= 3Fe3++2H2O+NO��
D����������Һ����μ���Ba(OH)2��Һ��Al3+�պó�����ȫ��
Al3+ +SO42��+Ba2+ +3OH��==BaSO4��+Al(OH)3��
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵�����ʾ��������ȷ����( )
A����ͬ�����£����������������������ֱ���ȫȼ�գ���Ӧ����ЧӦ��H1>��H2
B����C��ʯī����C�����ʯ����H=+1.9kJ/mol����֪���ʯ��ʯī�ȶ�
C����֪��101KPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ���������й�����ȼ���ȵ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2H2O��l����H=+285.8kJ/mol
D����ϡ��Һ�У�H+(aq)+OH��(aq)��H2O��l����H=��57.3kJ/mol��������0.5mol�����Ũ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶������У��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ҹ�����ʵʩ�ˡ��й�Ӫ�������ж��ƻ���������Ϊ����Ӫ����ƶѪ�����ڽ����м��뺬ij��Ԫ�ص�Ӫ��ǿ����������Ԫ����
A��ͭ B���� C���� D��п
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʼ����ͨ����ɫʯ����Һ�У��ܷ����ȱ�����ɫ�������
A��Na2O2 B��ϡ���� C��SO2 D��Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ��ˮ�ĵ���ﵽƽ�⣺H2O H++OH�� ��H>0������������ȷ���ǣ� ��
H++OH�� ��H>0������������ȷ���ǣ� ��
A����ˮ�м������������������ƣ�c(H+)����Kw����
B����ˮ�м��백ˮ��ƽ�������ƶ���c��OH-������
C����ˮ�м����������ͭ��ƽ�������ƶ���c��OH������С
D����ˮ���ȣ�KW����pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и�һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
�������������ʣ���NaOH��Һ ��Һ�� ��BaCO3���� ������KHSO4 ��Fe(OH)3���� ��ͭ��CO2 ��CH3COOH
��1���������������ڻ�������____________������ţ�
�������������ڷǵ���ʵ���____________������ţ�
��2�������ʢݽ���ͨ�磬�۲쵽����������������____________
���ϴ��������ܵ������___________������ţ�
��3��д���ٺ͢��ˮ��Һ��Ӧ�����ӷ���ʽ____________
��4��д���ܵĵ��뷽��ʽ____________
��5���������ܵ�ˮ��Һ�м��������ۣ�������Ӧ�����ӷ���ʽΪ____________
��6���ں�0.4mol�ٵ���Һ�л���ͨ���״����6.72LCO2�����屻��ȫ���գ���Ӧ���������___________���ѧʽ�����ù����ܵ����ӷ�Ӧ����ʽΪ____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����( )
A����ʳ���������е�Ħ����̼��ƣ�CaCO��2H��===Ca2����H2O��CO2��
B����������ˮ����Al(OH) 3���壺Al3����3H2O===Al(OH)3����3H��
C�������������Һ��ͨ������SO2��ClO����SO2��H2O===Cl����SO42-��2H��
D��Ca(HCO3) 2��Һ������NaOH��Һ��Ӧ��HCO3-��Ca2����OH-===CaCO3����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪�ֳ��������ѧУ�����ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
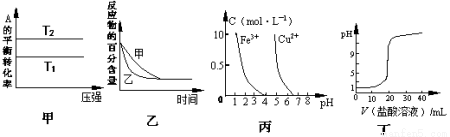
����ͼʾ���Ӧ�������������
A����ͼ�����жϣ���T1>T2����ӦA(g)+ B(g) 2C(g)�ġ�H<0
2C(g)�ġ�H<0
B��ͼ�ұ�ʾѹǿ�Կ��淴Ӧ2A(g)+2 B(g) 3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
C������ͼ��������ȥCuSO4��Һ�е�Fe3+��������Һ�м�������NaOH��Һ������pH��4
D��ͼ����ʾ��0��1mol/L������ζ�20mL 0��1mol/LNaOH��Һ����ҺpH�������������ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
Ԫ�����ڱ��Т�AԪ�ذ���C��Si��Ge��Sn��Pb�ȣ���֪Sn��+4���ȶ�����Pb��+2���ȶ��������ѧ֪ʶ���ж����з�Ӧ�У���Ӧ�����ԣ���ȷ���ǣ� ��
��Pb+2Cl2=PbCl4��Sn+2Cl2=SnCl4 ��SnCl2+Cl2=SnCl4��PbO2+4HCl=PbCl4+2H2O��Pb3O4+8HCl=3PbCl2+Cl2��+4H2O
A���٢ڢܢ� B���٢ڢۢ� C���٢ڢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com