
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
分析 (1)3s时处于平衡状态,平衡时二氧化碳为0.3mol,消耗的二氧化碳为0.4mol-0.3mol=0.1mol,二氧化碳转化率=$\frac{反应二氧化碳物质的量}{二氧化碳起始物质的量}$×100%;
(2)A.未指明正逆速率,不能确定是否处于平衡状态;
B.随反应进行,混合气体物质的量减小,恒温恒容下压强减小,容器内压强保持不变,说明到达平衡;
C.不同物质表示正逆速率之比等于化学计量数之比,反应到达平衡;
D.混合气体总质量不变,容器的容积不变,容器内密度始终不变;
(3)A.及时分离出产物,浓度降低,反应速率减低;
B.降低温度,反应速率降低;
C.增大反应物的浓度,反应速率增大.
解答 解:(1)3s时处于平衡状态,平衡时二氧化碳为0.3mol,消耗的二氧化碳为0.4mol-0.3mol=0.1mol,二氧化碳转化率=$\frac{0.1mol}{0.4mol}$×100%=25%,故答案为:25%;
(2)A.未指明正逆速率,不能确定是否处于平衡状态,若均为正反应速率,始终按该比例关系进行,若方便表示正逆速率,反应到达平衡,故A错误;
B.随反应进行,混合气体物质的量减小,恒温恒容下压强减小,容器内压强保持不变,说明到达平衡,故B正确;
C.由方程式可知υ逆(CO2)=υ逆(CH3OH),而 υ逆(CO2)=υ正(CH3OH),则 υ逆(CO2)=υ正(CO2),反应到达平衡,故C正确;
D.混合气体总质量不变,容器的容积不变,容器内密度始终不变,故D错误,
故选:BC;
(3)A.及时分离出产物,浓度降低,反应速率减低,故A错误;
B.降低温度,正逆反应速率均降低,故B错误;
C.增大反应物二氧化碳的浓度,反应速率增大,故C正确,
故选:C.
点评 本题考查化学平衡计算、平衡状态判断、反应速率影响因素等,比较基础,注意判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化,说明可逆反应到达平衡.


科目:高中化学 来源: 题型:选择题
| A. | +262.6 kJ•mol-1 | B. | -131.3 kJ•mol-1 | C. | +131.3 kJ•mol-1 | D. | -352.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
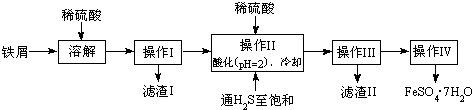
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +
+ $\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$
$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$ +H2O
+H2O| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日常生活中无水乙醇常用于杀菌消毒 | |
| B. | 用乙醇作萃取剂可以将碘从碘水中萃取出来 | |
| C. | 乙醇、乙烷和苯都可以与钠反应生成氢气 | |
| D. | 乙醇是一种可再生能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球插入蒸馏烧瓶中液体的液面以下 | |
| C. | 可用酒精萃取碘水中的碘 | |
| D. | 称量时,称量物放在托盘天平的右盘,砝码放在托盘天平的左盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.4mol | B. | 18.4mol•L-1 | C. | 20.4 | D. | 20.4mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com