
 (1)25℃时,部分弱酸的电离平衡常数如下表:
(1)25℃时,部分弱酸的电离平衡常数如下表:| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |


科目:高中化学 来源: 题型:
| A、-183 kJ/mol |
| B、-91.5 kJ/mol |
| C、+183 kJ/mol |
| D、+91.5 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 3 |
- 3 |
2- 3 |
- 3 |
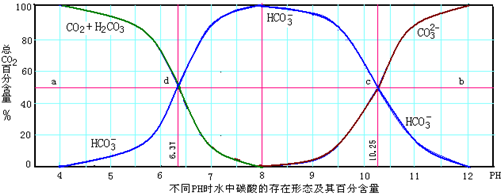
- 3 |
- 3 |
- 3 |
2- 3 |
2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 19.40 | 15.10 | 14.90 | 15.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2++2OH-=Cu(OH)2↓ CuCO3+2NaOH=Cu(OH)2↓+Na2CO3 |
| B、CO32-+2H+=CO2↑+H2O BaCO3+2HCl=BaCl2+CO2↑+H2O |
| C、Ca2++CO32-=CaCO3↓ Ca(NO3)2+NaCO3=CaCO3↓+NaNO3 |
| D、H++OH-=H2O Ba(OH)2+2HNO3=Ba(NO3)2+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com