
分析 钠投入到水中,发生反应方程式为:2Na+2H2O=2NaOH+H2↑,根据反应的化学方程式计算生成NaOH的质量、氢气质量,溶液的质量=钠的质量+水的质量-氢气质量,由此分析解答.
解答 解:将4.6g钠投入到97.8g水中,则:
2Na+2H2O=2NaOH+H2↑
46g 80g 2g
2.3g m(NaOH) m(H2)
m(NaOH)=$\frac{2.3g×80g}{46g}$=4.0g,物质的量为:$\frac{4.0g}{40g/mol}$=0.1mol,
m(H2)=$\frac{2.3g×2g}{45g}$=0.1g,体积为:$\frac{0.1g}{2g/mol}×22.4L/mol$=1.12L;则w(NaOH)=$\frac{4g}{2.3g+97.8g-0.1g}$×100%=4%,而溶液的体积为:$\frac{2.3+97.8-0.1}{1}×1{0}^{-3}$=0.1L,则溶液中溶质的物质的量浓度是$\frac{0.1mol}{0.1L}$=1mol/L,
答:(1)生成H2的体积为1.12L;
(2)所得溶液中溶质的质量分数为4%;
(3)溶液中溶质的物质的量浓度是1mol/L.
点评 本题考查化学方程式是计算、溶液质量分数的计算,题目难度不大,关键是计算溶液质量.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 阳光透过墙上的小孔在较暗的房间里形成一道道光柱 | |
| B. | 用石膏或盐卤制豆腐 | |
| C. | 向FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 | |
| D. | 长江三角洲的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在氧气中点燃 | |
| B. | 氮气与氢气在高温高压和有催化剂条件下反应 | |
| C. | 氢氧化钠溶液与盐酸混合 | |
| D. | 二氧化氮与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、HCO3-、SO42-、OH- | B. | Na+、Cu2+、Cl-、SO42- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Mg2+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
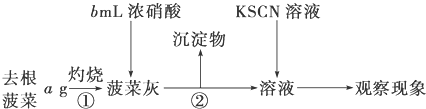
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
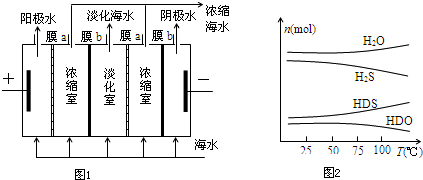
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCO3-+CO32-+3H+→2CO2↑+2H2O | B. | HCO3-+3CO32-+7H+→4CO2↑+4H2O | ||
| C. | 2HCO3-+CO32-+4H+→3CO2↑+3H2O | D. | CO32-+H+→HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com