
| A. | Si常用做信息高速公路的骨架--光导纤维的主要材料 | |
| B. | 测定NaOH熔点时,可以将NaOH放入石英坩埚中高温加热 | |
| C. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| D. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 |
分析 A.二氧化硅对光具有良好的全反射作用;
B.NaOH与二氧化硅反应;
C.煤通过气化、液化和干馏等可获得水煤气、甲醇以及苯等有机物;
D.二氧化硫有毒,不能漂白食品.
解答 解:A.二氧化硅对光具有良好的全反射作用,则二氧化硅为光导纤维的主要材料,故A错误;
B.NaOH与二氧化硅反应,不能将NaOH放入石英坩埚中高温加热,应选铁坩埚,故B错误;
C.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或者利用煤产生的H2和CO通过化学合成产生液体燃料或者其他液体化工产品的过程;煤的干馏是指隔绝空气加强热,使煤分解的过程,可以得到很多重要的化工原料,故C正确;
D.SO2可以用来漂白纸浆、毛、丝、草帽辫等,因二氧化硫有毒,不能用于增白食品,故D错误;
故选C.
点评 本题考查物质的性质、应用等,为高频考点,把握物质的性质、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意煤的综合应用及化学与生活的联系,题目难度不大.


科目:高中化学 来源: 题型:选择题
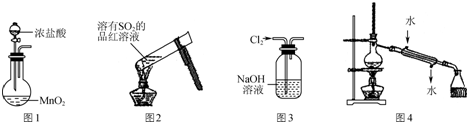
| A. | 实验室用图1装置制备Cl2 | |
| B. | 加热后图2中溶液颜色恢复红色 | |
| C. | 用图3装置除去Cl2中含有的少量HCl | |
| D. | 实验室用图4装置制取少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

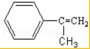 ;
;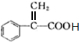 ;
;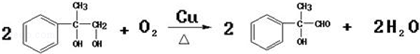 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32gO2和O3的混合气体所含质子数一定为16NA | |
| B. | 标准状况下,11.2LSO2中含有的分子数为0.5NA | |
| C. | 常温下,5.6 g铁与硝酸反应,失去的电子数一定为0.3 NA | |
| D. | 23g钠与足量氧气充分反应,转移的电子数一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
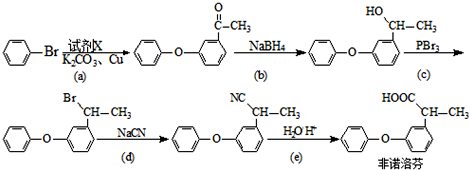
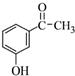 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
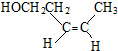 、(反式)
、(反式)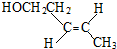 .若该单烯烃继续发生消去反应,生成的产物与溴单质按1:1的比例加成,得到的所有产物的结构简式(不考虑立体异构)为:CH2BrCHBrCH=CHCH3、CH2=CH-CHBrCHBrCH3、CH2Br-CH=CH-CHBr-CH3.
.若该单烯烃继续发生消去反应,生成的产物与溴单质按1:1的比例加成,得到的所有产物的结构简式(不考虑立体异构)为:CH2BrCHBrCH=CHCH3、CH2=CH-CHBrCHBrCH3、CH2Br-CH=CH-CHBr-CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
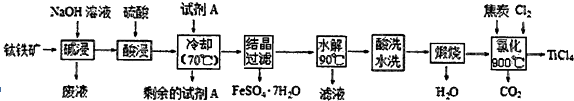
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com