
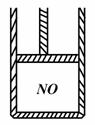
下图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)
 A. 等于1.369 g·L-1
A. 等于1.369 g·L-1
B. 等于2.054 g·L-1
C. 在1.369g·L-1和2.054g·L-1之间
D. 在2.054g·L-1和4.108g·L-1之间
【知识点】化学反应的可逆性;化学方程式的有关计算
【答案解析】D 解析:密闭容器存在反应:2NO+O2=2NO2,2NO2⇌N2O4,V(NO):V(O2)=2:1,第一个反应刚好反应,产生22.4ml的NO2,容器内气体总质量=原混合物质量=22.4÷22400×30+11.2÷22400×32=0.046(g),假设不存在第二个平衡,则反应后容器的体积为22.4ml,气体密度为0.046g÷0.0224L=2.05g/L;假设第二个反应完全反应,转化为N2O4,则容器内气体为11.2ml,则密度为0.046g÷0.0112L=4.108g/L,因为不能反应完全,所以密度应该在两个值之间
故答案选D


科目:高中化学 来源: 题型:
某氧化物的相对分子质量为a,其相同价态的硫酸盐的相对分子质量为b,则该元素的化合价的数值为:
A .(b-a)/20 B.(b-a)/40 C.(a -b)/80 D.(a-b)/20
查看答案和解析>>
科目:高中化学 来源: 题型:
向硝酸钠溶液中加入铜粉不发生反应,若再加入(或通入)某种物质,则铜粉可以逐渐溶解,不符合此条件的物质是
A.Fe(NO3)3 B. HCl C. NaHSO4 D. NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
现有阳离子交换膜、阴离子交换膜、石墨电极,请用氯碱工业中的膜技术原理,回答下列问题。
(1)写出氯碱工业中电解饱和食盐水的离子方程式 ;
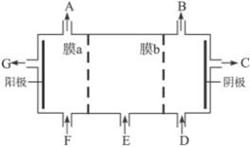
(2)请利用交换膜技术,根据上图框架,设计一个电解硫酸钠溶液制氢氧化钠溶液和硫酸溶液的装置,标出进出物质的化学式:
A_________;C_________; E_________;膜b为 离子交换膜(填“阳”或“阴”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
①铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+
②Cu(OH)2和HNO3混合:H++OH-===H2O
③Fe与稀硝酸反应 Fe+2H+==Fe2++H2↑
④H2SO3与氢氧化钠混合 H++OH-==H2O
⑤碳酸钡与稀盐酸反应: BaCO3+2H+==Ba2++H2O+CO2↑
⑥SO3溶于水:SO3+H2O==2H++SO42-
A.③⑤⑥ B.⑤⑥ C.①③④ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
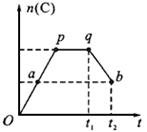
向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如下图所示,试回答:
 (1)a点之前的反应的离子方程式为________________。
(1)a点之前的反应的离子方程式为________________。
(2)a点到b点之间的反应的离子方程式是________________。
(3)c点二氧化碳体积是________L。
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
B.温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变
C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<0,则该反应一定能自发进行
D.由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com