
【题目】有下列盐:①FeCl3 ②CH3COONa ③NaCl,其水溶液的pH由大到小排列正确的是
A. ①>③>②B. ②>③>①C. ③>②>①D. ①>②>③
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
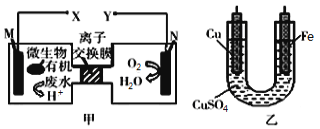
A.质子透过离子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极反应式:(C6H10O5)n+7nH2O-24ne-=6nCO2↑+24nH+
D.当N电极消耗0.25mol气体时,则铁电极增重16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《天工开物》第七卷《陶埏(陶瓷)》中记载“水火既济而土合……后世方土效灵,人工表异,陶成雅器,有素肌、玉骨之象焉”,以上所述的“陶成雅器”的主要原料是
A. 黏土 B. 纯碱、石灰石、石英砂
C. 黏土、石灰石 D. 二氧化硅、硅酸钙、硅酸铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示,D的相对分子质量与E相差42,请回答下列问题;
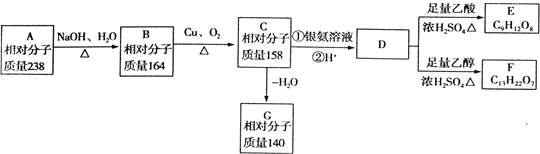
(1)D中含有的官能团是_________,各种官能团的个数比是________。
(2)D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,请写出D的结构简式__________。
(3)写出B生成C的化学方程式______________________________________.
(4)A只含一种官能团,则A的结构简式为___________。
(5)芳香族化合物H与G互为同分异构体,1molH与足量的钠反应产生1.5molH2,与足量的氢氧化钠溶液反应消耗2molNaOH,且H苯环上的一氯代物只有两种,写出符合条件的H的结构简式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于吸热反应的是
A. 镁跟盐酸反应 B. 乙醇的燃烧
C. 盐酸与氢氧化钠溶液反应 D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
A. c(NH4+)=c(SO42﹣)
B. c(NH4+)>c(SO42﹣)
C. c(NH4+)<c(SO42﹣)
D. c(OH﹣)+c(SO42﹣)=c(H+)+c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在工业合成中广范应用。
(1)通过下列反应可以制备甲醇:
CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.8kJ/mol,
CH3OH(g) ΔH=-90.8kJ/mol,
CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH=+41.3kJ/mol
CO(g)+H2O(g) ΔH=+41.3kJ/mol
请写出由CO2和H2制取甲醇的热化学方程式______________。
(2)己知合成氨的反应为:N2+3H2![]() 2NH3 △H<0。某温度度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和怛容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请冋答下列问题:
2NH3 △H<0。某温度度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和怛容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请冋答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是________(用a、b、c表示)。
②曲线a条件下该反应的平衡常数K=_____________。
③b容器中M点,v(正)________v(逆)(填“大于”、“小于”或“等于”)。
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为________;标准状况下,当阴极收集到11.2LN2时,理论上消耗NH3的体积为_____________。
(4)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中c(NH4+)____ c(HCO3-) (填“>”、“<”或“=”);反应NH4++HCO3-+H2O![]() NH3H2O+H2CO3的平衡常数K=_______。
NH3H2O+H2CO3的平衡常数K=_______。
(已知常温下NH3H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7, K2=4×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,属于同分异构体的是
A.O2和O3
B.CH2=CHCH2CH3和CH3CH=CHCH3
C. CH3CH2OH和CH3OCH3
D. CH3CH2CH3和CH3(CH2)2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com