
(双选)向某密闭容器中加入0 .3 molA 、0 .1 molC 和一定量的 B 三种气体。一定条 件下发生反应,各物质浓度随时间变化如甲图所示[t0~ t1阶段 c ( B)未画出]。附图乙为 t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件并且所用条件均不同。已知,t3~t4阶段为使用催化剂。下列说法正确的是 ( )
件下发生反应,各物质浓度随时间变化如甲图所示[t0~ t1阶段 c ( B)未画出]。附图乙为 t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件并且所用条件均不同。已知,t3~t4阶段为使用催化剂。下列说法正确的是 ( )
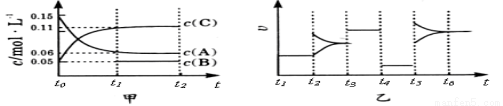
A.若t1=15 s,生成物C在t0~t1时间段的平均反应速率为0.004mol·L-1·s-1
B.t4~t5阶段改变的条件为降低反应温度
C.B的起始物质的量为 0.02mol
D.t5~t6阶段容器内A的物质的量减少0.03 mol,而此过程中容器与外界的热交换总量为akJ,该反应的热化学方程式为3A(g) B(g)+2C(g) ΔH=+100akJ·mol-1
B(g)+2C(g) ΔH=+100akJ·mol-1
科目:高中化学 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
己知维生素A的结构简式可写为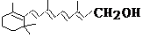 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
A.维生素A的分子式为C20H32O
B.维生素A不能使溴的四氯化碳溶液褪色
C.该有机物能发生取代反应
D.1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,实验装置如图1所示.电解过程中的实验数据如图2所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标况).则下列说法中正确的是( )
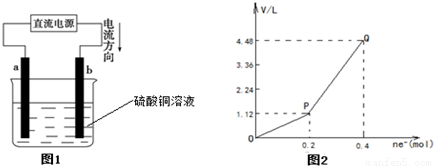
A.电解过程中,b电极表面先有红色物质析出,然后才有气泡产生
B.从开始到Q点时收集到的混合气体的平均相对分子质量为17
C.曲线OP段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化
D.a电极上发生反应的方程式为:2H++2e-═H2↑和4OH--4e-═2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:选择题
俄罗斯科学家用含20个质子的钙的一种核素轰击含95个质子的镅元素,结果4次成功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是( )
A. 115号元素衰变成113号元素是化学变化
B. 核素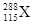 的中子数为173
的中子数为173
C. 113号元素最高正价应为+5
D. 115号与113号元素的原子质量比为115:113
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二上开学测化学卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行如下可逆反应X(g)+Y(g)  Z(g)+W(s) ΔH>0。下列叙述中,正确的是( )
Z(g)+W(s) ΔH>0。下列叙述中,正确的是( )
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.改变条件,又达新平衡,此时上述反应的平衡常数K值一定增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二上开学测化学卷(解析版) 题型:选择题
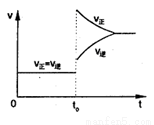
(双选)往一个体积不变的密闭容器中充入H2和I2发生反应H2(g)+I2(g) 2HI(g) △H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )
2HI(g) △H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )
A.容器内气体颜色变浅,平均相对分子质量不变
B.平衡不移动,混合气体密度增大
C.H2的转化率增大,HI平衡浓度变小
D.改变条件前后,速率图象如图
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.4周考化学卷(解析版) 题型:计算题
在一密闭的2L容器里装有4molSO2和2molO2,在一定条件下开始反应。2min 末测得容器中有1.6molSO2。请计算① 2min 末SO3的浓度;②2min 内O2的平均反应速率。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.4周考化学卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.c(NH4+)相等的(NH4)2SO4溶液、NH4HSO4溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2SO4] <c[NH4HSO4]<c(NH4Cl)
B.欲除去CuC12溶液中混有少量的FeC13,可加入CuO
C.0.2 mol/LHCl溶液与等体积0.05mol/LBa(OH)2溶液混合后,溶液的pH=1
D.0.2mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一入学考试化学卷(解析版) 题型:填空题
为了测定某氯酸钾与二氧化锰混合物中氯酸钾的质量分数,课外小组的同学设计了如下实验:取3.0g 混合样品放入如图所示的大试管中,充分加热,直到反应完全,并用如图所示装置测量出生成氧气的体积。试回答下列问题:
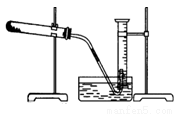
(1)如何检查装置的气密性?
(1)现有如下可供选择的操作:①将导气管放入盛满水的量筒内;②给药品加热;③有连续气泡产生时开始收集气体;④取出导气管;⑤反应完全后停止加热(如图,此时导管出口略高于液面);⑥冷却至室温;⑦调整量筒内外液面高度使之相同后读出量筒内气体体积数。
为了较准确地测量出生成的氧气在常温、常压下的体积,正确的操作顺序是(填序号)______________。
(3)为了较准确地测量到气体的体积,需要调整量筒内外液面高度,其原理是:____________________。
(4)在常温常压下共收集到气体680mL(此时氧气密度为1.41g·L-1),其质量为_______g,原混合物中氯酸钾的质量分数约是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com