
【题目】室温下,在pH=12的某溶液中,分别有甲、乙、丙、丁四位同学计算出由水电离出的c(OH-)的数据分别为甲:1.0×10-7 mol·L-1;乙:1.0×10-6 mol·L-1;丙:1.0×10-2 mol·L-1;丁:1.0×10-12 mol·L-1。其中你认为可能正确的数据是( )
A.甲、乙B.乙、丙C.丙、丁D.乙、丁
【答案】C
【解析】
pH=12,说明溶液显碱性,则溶液可能为碱溶液,也有可能是强碱弱酸盐溶液,以此根据水的离子积常数进行计算。
pH=12,说明溶液显碱性,则该溶液可能为碱溶液,也有可能是强碱弱酸盐溶液;
1.若是碱溶液,c(H+)=1.0×10-12mol/L,碱溶液中氢离子来源于水的电离,由水电离出的氢离子与氢氧根离子相等,故由水电离出的c(OH-)=1.0×10-12mol/L,则丙正确;
2.若是强碱弱酸盐溶液,c(H+)=1.0×10-12mol/L,c(OH-)=![]() =1.0×10-2mol/L,强碱弱酸盐溶液中氢氧根离子来源于水的电离,故由水电离出的c(OH-)=1.0×10-2mol/L,则丁正确;
=1.0×10-2mol/L,强碱弱酸盐溶液中氢氧根离子来源于水的电离,故由水电离出的c(OH-)=1.0×10-2mol/L,则丁正确;
故可能正确的数据是丙、丁;故合理选项是C。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】用电解法处理含![]() 的废水,探究不同因素对含
的废水,探究不同因素对含![]() 废水处理的影响。结果如表所示(
废水处理的影响。结果如表所示(![]() 的起始浓度、体积、电压、电解时间均相同)。下列说法错误的是 ( )
的起始浓度、体积、电压、电解时间均相同)。下列说法错误的是 ( )

A.实验ⅱ与实验ⅰ对比,其他条件不变,增加c(H+)有利于![]() 的去除
的去除
B.实验ⅲ与实验ⅱ对比,其他条件不变,增加c(Fe3+)有利于![]() 的去除
的去除
C.实验ⅲ中Fe3+循环利用提高了![]() 的去除率
的去除率
D.若实验iV中去除0.0l mol ![]() ,电路中共转移0.06 mol电子
,电路中共转移0.06 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态化合物AB会发生微弱的自身电离,电离方程式为AB![]() A++B-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是( )
A++B-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.c(A+)随温度升高而降低B.在35 ℃时,c(A+)>c(B-)
C.AB的电离程度(25℃)>(35℃)D.AB的电离是吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种有机化合物的结构简式如图所示。有关该物质的说法中正确的是( )
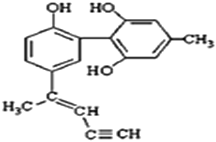
A.该物质有四种官能团,其中一种名称为羟基
B.该分子中的所有碳原子不可能共平面
C.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
D.1 mol该物质与H2反应时最多消耗H2 9 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由物质a为原料,制备物质d(金刚烷)的合成路线如下图所示:
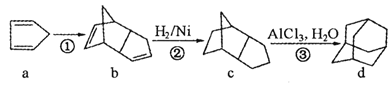
关于以上有机物的说法中,不正确的是
A. a分子中所有原子均在同一平面内 B. a和Br2按1:1加成的产物有两种
C. d的一氯代物有两种 D. c与d的分子式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是地球上组成生命的最基本的元素之一。按要求回答:
![]() 碳原子核外有________种不同空间运动状态的电子
碳原子核外有________种不同空间运动状态的电子
![]() 碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体
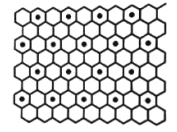
碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体![]() 如图
如图![]() ,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有_________个。
,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有_________个。
![]() 碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。![]() 吡啶分子中含有
吡啶分子中含有![]() 键数目是__________。
键数目是__________。
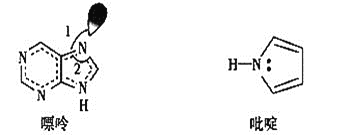
![]() 嘌呤结构中N原子的杂化方式为________。
嘌呤结构中N原子的杂化方式为________。
![]() 嘌呤中轨道之间的夹角
嘌呤中轨道之间的夹角![]() 比
比![]() 大,解释原因___________。
大,解释原因___________。
![]() 将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构
将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构![]() 碳。已知
碳。已知![]() 碳密度为
碳密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]() ,则
,则![]() 碳的晶胞参数
碳的晶胞参数![]() ________
________![]() 写出表达式即可
写出表达式即可![]() 。
。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为_________(填标号)。C、D中有气泡冒出,并可观察到的现象分别为_______________。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu及化合物在生产、国防中有重要的应用。
I.纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:Cu2O(s)+![]() O2(g)=2CuO(s) ΔH=-196kJ·mol-1
O2(g)=2CuO(s) ΔH=-196kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220.8kJ·mol-1
则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为___。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢制取甲醛:CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
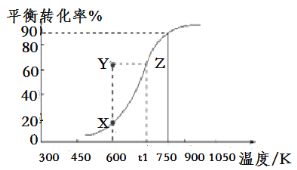
①该反应的ΔH___0(填“>”或“<”);600K时,Y点甲醇的v(正)___v(逆)(填“>”或“<”)。
②在t1K时,向固定体积为1L的密闭容器中充入2molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)___,温度为t1时,该反应的平衡常数K的表达式为___。
II.Cu既是常见的催化剂,又是常见的电极材料。
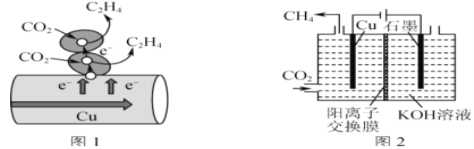
(3)图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当直接传递的电子物质的量为2mol时,则参加反应的CO2的物质的量为___。
(4)图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为___。
III.含铜离子的废水会造成污染,通常将其转化为硫化铜沉淀而除去。
(5)已知:Ksp(CuS)=1×10-36,要使铜离子的浓度符合排放标准(不超过6.25×10-6mol/L),溶液中的硫离子的物质的量浓度至少为___mol/L(保留至小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验某溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作.其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是![]()
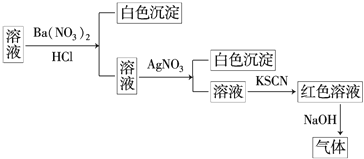
A.原溶液中一定含有![]() B.原溶液中一定含有
B.原溶液中一定含有![]()
C.原溶液中一定含有![]() D.原溶液中一定含有
D.原溶液中一定含有![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com