
离子检验的常用方法有三种:
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法不合理的是
A NH4+-气体法 B I--沉淀法
C Fe3+-显色法 D Ca2+-气体法
科目:高中化学 来源: 题型:
下列实验能达到目的的是( )
A.在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜以加快反应速率
C.用玻璃棒搅拌漏斗中的液体以加快过滤速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
取化学式为MZ的黄色粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水。按图连接仪器。
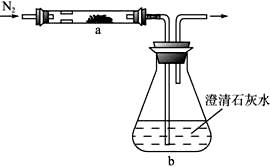
实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。根据以上叙述回答问题:
(1)元素Z是 :
(2)停止加热前是否需要先断开a和b的连接处?为什么?
;
(3)反应管a中发生的所有反应的化学方程式是
;
(4)本实验的尾气是否需处理?如需处理,请回答如何处理:如不需处理,请说明理由。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1:该混合金属粉末中除铝外还含有 元素;
假设2:该混合金属粉末中除铝外还含有 元素;
假设3:该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
| ③ | ||
| ④ | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组设计出图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
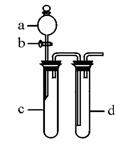
(固定装置略去)
(1)实验前,活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
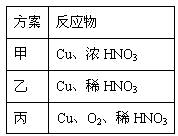
(3)题27表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是______________ 。
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象为 ;但此实验的不足之处是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水蒸气通过灼热的焦炭后,流出气体的主要成分是CO和H2,还有CO2和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气中有CO和H2。(加热装置和导管等在图中略去)
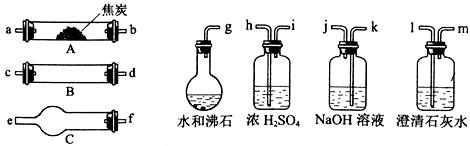
回答下列问题:
(1)盛浓H2SO4的装置用途是 ,盛NaOH溶液的装置用途是 。
(2)仪器B中需加入试剂的名称(或化学式)是: ,所发生反应的化学方程式是: 。
(3)仪器C中需加入试剂的名称(或化学式)是: ,其目的是 。
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:g—ab—  。
。
(5)能证明混合气中含有CO的实验依据是 。
(6)能证明混合气中含有H2的实验依据是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是 ( )
A.在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸
B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜加快反应速率
C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
碘与氢气反应的热化学方程式是
①I2(g)+H2(g) 2HI(g)ΔH=-9.48 kJ·mol-1 ②I2(s)+H2(g)
2HI(g)ΔH=-9.48 kJ·mol-1 ②I2(s)+H2(g) 2HI(g)ΔH=+26.48 kJ·mol-1 下列说法正确的是( )
2HI(g)ΔH=+26.48 kJ·mol-1 下列说法正确的是( )
A. 从上述两反应可知1mol的I2(g)能量比1mol的I2(s)能量高
B. I2(s) I2(g) ΔH<0
I2(g) ΔH<0
C. ②的反应物总能量与①的反应物总能量相等
D. 1 mol I2(g)中通入1 mol H2(g),发生反应时放出的热量为9.48 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com