
(16分).联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。(1)已知:2NO2(g) N2O4(g),N2O4为无色气体。
N2O4(g),N2O4为无色气体。
① 在上述条件下反应能够自发进行,则反应的ΔH 0(填写“>”、“<”、“=”)
② 一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡,达到平衡状态的标志 。
N2O4(g)达到平衡,达到平衡状态的标志 。
A单位时间内生成n mol N2O4的同时生成2 nmolNO2
B用NO2、N2O4的物质的量浓度变化表示的反应速率之比为2:1的状态
C混合气体的颜色不再改变的状态
D混合气体的密度不再改变的状态
E混合气体的平均相对分子质量不再改变的状态
③ 其他条件不变时,下列措施能提高NO2转化率的是 (填字母)
A.减小NO2的浓度 B.降低温度 C.增大压强 D.升高温度
(2)25℃时,1molN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放612.5 kJ的热量。请写出该反应的热化学方程式: 。
(3) 17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时,c(NO2)=0.2 mol·L-1,
c(N2O4)=0.16 mol·L-1。则反应初始时,充入NO2的物质的量为 ;NO2的转化率为 ;该温度下该反应的平衡常数K为 ;该温度下反应N2O4(g)  2NO2(g)的平衡常数K为 。
2NO2(g)的平衡常数K为 。
(1)① < ② ACE ③ BC
(2) 2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) △H=-1225KJ/mol (12分)
(3) 5.2mol 62% 4 1/4
【解析】
试题分析:(1)①根据反应自发进行时焓减熵增的原则,2NO2(g) N2O4(g)是熵减的反应,若反应能够自发进行,则焓减即反应的ΔH<0;
N2O4(g)是熵减的反应,若反应能够自发进行,则焓减即反应的ΔH<0;
②A、单位时间内生成n mol N2O4的同时生成2 nmolNO2,表示正逆反应速率相等,是平衡状态的标志,正确;B、用NO2、N2O4的物质的量浓度变化表示的反应速率之比为2:1的状态不是平衡状态,因为在反应未达平衡时也符合此规律,错误;C、二氧化氮是红棕色气体,反应未达平衡时气体的颜色一直变化,达平衡时不再变化,正确;D、恒容密闭容器中,容器的体积不变,气体的质量不变,所以气体的密度始终不变,不是平衡的标志,错误;E、该反应是气体的物质的量变化的可逆反应,气体的相对分子质量一直变化,当达到平衡时,气体的相对分子质量不再变化,正确,答案选ACE;
③A 、减小NO2的浓度,平衡逆向移动,二氧化氮的转化率降低,错误;B 、降低温度,平衡正向移动,二氧化氮的转化率增大,正确;C 、增大压强,平衡正向移动,二氧化氮的转化率增大,正确;D、 升高温度,平衡逆向移动,则二氧化氮的转化率降低,错误,答案选BC;
(2)根据题意N2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l)的热化学方程式为2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) △H=-1225KJ/mol;
(3)生成0.16mol/L的N2O4,则消耗0.32mol/L的NO2,所以反应初始时,充入NO2的物质的量为(0.2+0.32)mol/L×10L=5.2mol;NO2的转化率是0.32mol/L×10L/5.2×100%=62%;该温度下该反应的 平衡常数K=0.16 /0.22 =4;逆反应的平衡常数与正反应的平衡常数互为倒数,所以该温度下反应N2O4(g)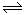 2NO2(g)的平衡常数K为1/4.
2NO2(g)的平衡常数K为1/4.
考点:考查化学平衡理论的应用,平衡常数的计算,平衡移动的判断,热化学方程式的书写


科目:高中化学 来源:2014-2015学年甘肃省天水市高二上学期期中考试化学试卷(解析版) 题型:选择题
现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a ,则碳的质量分数是( )
A.6(1-a)/7 B.3a/4
C.(1-a)/7 D.12 (1-a)/13
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高一上学期期中考试化学试卷(解析版) 题型:选择题
对危险化学品要在包装标签上印上警示性标志。下列化学品名称与警示标志名称对应正确的是
A.酒精—剧毒品 B.浓硫酸—腐蚀品 C.氯化钠—易燃品 D.烧碱—剧毒品
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃甘谷县第一中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
相等物质的量的CO和CO2的下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3 ④所含的C原子数目之比为1:1
⑤它们的质量之比为7:11
A.①② B.②③ C.④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃甘谷县第一中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
乘车前都要进行安检,易燃、易爆、剧毒、易腐蚀、强氧化剂等物品严禁上车。下列物品可让乘客带上车的是( )
①浓硫酸 ②氰化钾 ③水银 ④汽油 ⑤黑火药 ⑥白磷 ⑦酒精
A.①④⑤ B.①②⑥⑦ C.①③④⑤⑦ D.全部都不能带上车
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃天水市高二上第一阶段考试卷化学试卷(解析版) 题型:选择题
1g H2燃烧生成液态水放出142.9 kJ的热量,下列热化学方程式书写正确的是( )
A.2H2(g)+ O 2(g) = 2H2O (1), ΔH = —142.9 kJ·mol-1
B.2H2(g)+ O 2(g) = 2H2O (1), ΔH = —571.6 kJ·mol-1
C.2H2+O2 = 2H2O, ΔH = —571.6 kJ·mol-1
D.H2(g)+  O 2(g) = H2O (1), ΔH = +285.8 kJ·mol-1
O 2(g) = H2O (1), ΔH = +285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃天水市高二上第一阶段考试卷化学试卷(解析版) 题型:选择题
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+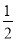 O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
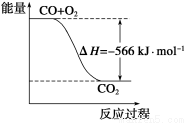
A.CO的燃烧热为283 kJ
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-532kJ·mol-1
D.CO2(g)与Na2O2(s)反应放出532 kJ热量时,转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南长沙市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列各组物质的性质比较中,正确的是
A.酸性:HClO4>H3PO4>H2SO4
B.氢化物的稳定性:H2S>HF>H2O
C.碱性:Al(OH)3>Mg(OH)2>NaOH
D.氧化性:F2>C12>Br2>I2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:选择题
反应A(g)+B(g) 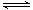 C(g)+D(g)过程中的能量变化如图所示,
C(g)+D(g)过程中的能量变化如图所示,
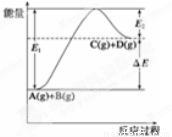
①正反应为放热反应,
②反应物总能量低于生成物总能量,
③反应物的总键能小于生成物的总键能,
④1molA与1molB充分反应后,能量变化为ΔE,
⑤加入催化剂后,反应加快,ΔE减小,
⑥反应达到平衡时,升高温度,A的转化率增大,
⑦升高温度可增大正反应速率,降低逆反应速率,
⑧E2是反应C(g)+D(g) 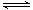 A(g)+B(g) 的活化能,
A(g)+B(g) 的活化能,
以上有关说法正确的是
A.⑤⑥⑦⑧ B.①②③④ C.①③⑤⑦ D.②⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com