
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
1.写出铬原子的基态的核外电子排布式___________________
2.在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有 (填序号),CS2分子的空间构型是_______ ___。
科目:高中化学 来源: 题型:
某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应。资料显示 :镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案并验证产物、探究反应原理。
:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案并验证产物、探究反应原理。
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能为____________________。
猜测2:可能为MgCO3。
猜测3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 预期现象和结论 |
|
| 将实验Ⅰ中收集的气体点燃 | |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量________ | ________________;白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀;溶液中存在________离子 |
(3)设计定量实验确定实验Ⅰ的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物31.0 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8 g,装置B增重13.2 g,试确定白色不溶物的化学式_________________。
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡的原因__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.氟化氢水溶液中存在的氢键有4种
B.H—O键键能为463 kJ·mol-1,即18 g 气态水分解成H2和O2时,消耗能量为2×463 kJ
C.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,观察现象可比较26Al、26Mg金属性强弱
D.室温下,V1 L pH=3的硫酸与V2LpH=11的NaOH溶液溶液混合,忽略分子间间隙引起的体积变化,若混合后溶液pH=4,则V1:V2=11:9
查看答案和解析>>
科目:高中化学 来源: 题型:
.X、Y、Z三种短周期元素,X元素的原子最外层只有一个电子,Y元素的原子M电子层的电子数为K、L上电子总数的一半, Z元素的原子L层电子数比Y原子L层电子数少2个,由这三种元素组成的化合物的化学式可能是( )。
A.X3YZ4 B.X2YZ3 C.XYZ2 D.X2YZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:

则下列有关比较中正确的是( )
A.第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中前7周期的元素种数如下:
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
请分析周期表与元素种数的关系,然后预言第8周期最多可能含有的元素种数( )
A.18 B.32 C.50 D.64
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的 质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是 ( )
①w=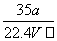 ×100% ②c=
×100% ②c=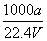 ③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH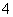 )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com