
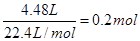 ��
��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����������ֻ��SO42- |
| B������4molCu2S���μӷ�Ӧ������Ϊ5mol |
| C������4mol����ת�ƣ���������ͭ��0.4mol |
| D����ƽ��H2O���ӵļ�����Ϊ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
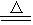 MnCl2��Cl2�� �� 2H2O��
MnCl2��Cl2�� �� 2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| | ѡ���Լ� | ʵ������ |
| ����1 | | |
| ����2 | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 TiCl4��2CO������ TiCl4��2Mg
TiCl4��2CO������ TiCl4��2Mg 2MgCl2��Ti
2MgCl2��Ti| A����Ӧ�����û���Ӧ | B����Ӧ���Ǹ��ֽⷴӦ |
| C����Ӧ����TiO2������������������������ | D����Ӧ���н���þ�ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
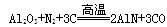 ������������ȷ���� ( )
������������ȷ���� ( )| A��AlN�е��Ļ��ϼ�Ϊ+3 |
| B��AlN��Ħ������Ϊ41 g |
| C��������Ӧ�У�N2����������Al2O3 �Ȳ���������Ҳ���ǻ�ԭ���� |
| D��������Ӧ�У�ÿ����1 mol AlN��ת��6 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���٢� | C���ۢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Mn��CN��2 + ��CN��2�� + 2H2O
Mn��CN��2 + ��CN��2�� + 2H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com