
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 |
中的物质 |
中的物质 |
收集的气体 |
|
| 浓氨水 |
|
|
|
| 浓硫酸 |
|
|
|
| 稀硝酸 |
|
|
|
| 稀盐酸 |
|
|
|
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】处于下列状态的物质中:①氯化钠固体 ②干冰 ③HCl气体 ④铜 ⑤硫酸钡固体 ⑥蔗糖 ⑦乙醇 ⑧熔融的硝酸钾 ⑨NaCl溶液
(1)能导电的是(填编号,下同) ;
(2)属于电解质的是 ;
(3)属于非电解质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3CH2CH2CH3(正丁烷)和(CH3)2CHCH3(异丁烷)的关系是
A. 同分异构体 B. 同素异形体 C. 同位素 D. 同一种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列试题给予的信息,回答问题。
(1)某烃是一种常用的化工原料,可用于制造炸药、农药、苯甲酸、染料、合成树脂及涤纶等。下图是该烃分子的球棍模型,则该烃的分子式是________,其一氯代物有________种。
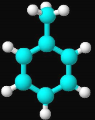
(2)分子中有6个甲基,而一溴代物只有1种的烷烃,结构简式是____________。
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
![]()
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,与水加成时,生成的主要产物为C,且B 中仅含有4个碳原子、1个溴原子、1种氢原子,则B的结构简式为__________, A与水在催化剂存在下发生加成反应的化学方程式为_________________(只写主要产物)。
(4) 某气态烷烃和一气态烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L,通入足量的溴水,溴水质量增加2.8g,此两种烃的组成为__________和___________(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应在不同反应时间各物质的物质的量的变化情况如下图所示。

回答下列问题:
(1)该反应的反应物是________,生成物是________,化学方程式为_____________________。
(2)反应开始至2 min时,能否用C的浓度变化来计算反应速率?为什么?________________________________________________________________________。
(3)2 min后,A、B、C的物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了______________状态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类最早使用的金属之一。
(1)铜元素基态原子的价电子排布式为_______,其核外能级能量的高低3d______4s(填“>”、“<”或“=”)
(2)Cu与元素A能形成如下图所示的两种化合物甲和乙。元素A是短周期非金属元素,A的常见氧化物常温下为液态,其熔沸点比同主族其他元素的氧化物高。
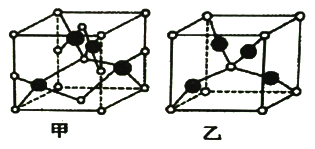
① 两种化合物的化学式分别为:甲___________,乙___________。
② 热稳定性甲_________乙(填“>”、“<”或“=”),试从原子结构上解释原因____。
(3)铜离子形成的某种配合物阳离子具有轴向狭长的八面体结构(如下图)。
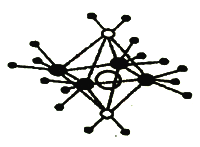
已知两种配体都是10电子的中性分子,且都含氢元素。
① 两种配体分子的配位原子电负性大小为______(填元素符号),其中热稳定性较弱的配体为(用电子式表示)__________。
② 该配合物阳离子与SO42-形成的配合物X的化学式为_________.
(4)Cu单质的晶体为面心立方堆积,其晶胞立方体的边长为acm, Cu的相对原子质量为63.5,单质Cu的密度为ρg/cm3,则阿伏加德罗常数可表示为_____mol-1(含“a、ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示几种无机物之间的转换关系。其中A、B均为黑色粉末,B为非金属单质,C为无色无毒气体,D为金属单质,E是红棕色气体,G是具有漂白性的气体,H的水溶液呈蓝色。
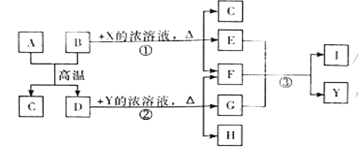
请回答下列问题:
(1)A的化学式是 ,C的电子式是 ,Y的名称是 。
(2)反应1的化学方程式为 。
(3)19.2g的D与足量的一定浓度X的溶液反应,将所得到的气体与 LO2(标准状况下)混合,恰好能被水完全吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素A、B、C、D、E的原子序数依次增大,A的质子数等于周期数,B与C的 P轨道均有三个成单电子,D的最高正价与最低负价代数和为4,E的最外层只有一个电子, 内层轨道处于全充满状态。试回答下列问题。
(1)基态E原子的电子排布式为_________;C和D的第一电离能较大的________(填元素符号)。
(2)DO32-中D原子的杂化类型为_________;A、D和氧元素组成的液态化合物A2DO4中存在的作用力有_____________。
(3)结构式为A—B=B—A的分子中σ键和π键的数目比为________;B2分子和NO+离子互为等离子体,则NO+的电子式为___________。
(4)向EDO4溶液中加入过量稀氨水,其化学方程式为_______________;产物中阳离子的配体是_____________(填化学式)。
(5)D(黑球)和E(白球)形成某种晶体的晶胞如图所示。已知该晶体的晶胞边长为516Pm,则黑球和白球之间最近距离为________pm(精确到0.1,已知![]() =1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因__________。
=1.732)若ED中D2-被O2-代替,形成的晶体只能采取NaCl型堆积,试从晶体结构分析其不同及原因__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com