
【题目】(1)常温下将0.2 mol/LHCl溶液与0.2 mol/LMOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)__________0.2 mol/LHCl溶液中由水电离出的c(H+)。(填“>”“<”或“=”),该混合溶液的物料守恒式为 。
(2)常温下若将0.2 mol/LMOH溶液与0.1 mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__________MCl的水解程度。(填“>”“<”或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH__________。(填“>7”“<7”或“无法确定”)
(4)纯碱溶液呈碱性的原因(用离子方程式表示)__________________________,纯碱溶液离子浓度由大到小的顺序为 。
(5)某温度时,测得0.01 mol/L的NaOH溶液pH为11,在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合。若所得混合溶液为中性,且a=12,b=2,求Va ∶Vb = 。
【答案】(1)> c(Cl-)=c(MOH)+c(M+)(2)<(3)<7
(4)CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
(5)1:10
【解析】
试题分析:(1)常温下将0.2 mol/LHCl溶液与0.2 mol/LMOH溶液等体积混合恰好反应生成MCl和水,测得混合溶液的pH=6,这说明M+水解,促进水的电离,溶液显酸性,则混合溶液中由水电离出的c(H+)>0.2 mol/LHCl溶液中由水电离出的c(H+)。该混合溶液的物料守恒式为c(Cl-)=c(MOH)+c(M+)。
(2)常温下若将0.2 mol/LMOH溶液与0.1 mol/LHCl溶液等体积混合,这说明生成的MCl和剩余的MOH的浓度相等,测得混合溶液的pH<7,溶液显酸性,则说明在相同条件下MOH的电离程度<MCl的水解程度。
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,这说明HR一定是弱酸,反应后HR过量,则混合溶液的pH<7。
(4)碳酸钠水解,溶液显碱性,反应的离子方程式为CO32-+H2O![]() HCO3-+OH-,因此纯碱溶液离子浓度由大到小的顺序为 c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。
HCO3-+OH-,因此纯碱溶液离子浓度由大到小的顺序为 c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。
(5)某温度时,测得0.01 mol/L的NaOH溶液pH为11,则该温度下Kw=10-13。在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合。若所得混合溶液为中性,则![]() ,且a=12,b=2,因此Va ∶Vb =1:10。
,且a=12,b=2,因此Va ∶Vb =1:10。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子中,在给定条件下能够大量共存的是
A. 通入足量SO2气体后的溶液中:H+、Ca2+、Fe3+、NO3-
B. 无色溶液中:Al3+、NH4+、Cl-、S2-
C. 使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3-
D. c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素在周期表中的位置取决于( )
A.元素原子核内的中子数
B.元素的最高正化合价
C.元素原子的电子层数
D.元素原子核外的电子层数和最外层上的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaH与水反应的化学方程式为NaH+H2O=NaOH+H2↑,下列有关该反应的说法正确的是
A. H2O是还原剂 B. NaH被还原
C. H2O失去电子 D. NaH发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红矾钠(重铬酸钠:![]() )是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:
)是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:
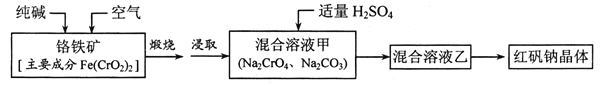
请回答下列问题:
(1)![]() 的基态电子排布式为____________。
的基态电子排布式为____________。
(2)锻烧铬铁矿发生反应:____________![]() 配平上述化学反应方程式。
配平上述化学反应方程式。
(3)溶液甲中加入H2SO4时,可以观察到溶液由黄色变为橙色,并放出无色气体,有 关反应的离子方程式为____________。
(4)制备红矾钠的废水必须进行处理。首先酸化废水,将含+6价铬的酸性废液放入电解槽内,用铁作阳极进行电解,阴极析出H2,阳极产物被![]() 氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
①阳极的电极反应式为(不考虑后续反应):____________。
②溶液中金属离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因:______。
③已知某含![]() 的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,该条件下向100 mL的CaSO4饱和溶液中,加入200 mL 0.03 mol·L -1 的Na2SO4溶液,针对此过程的下列叙述正确的是(忽略混合过程中的体积变化)
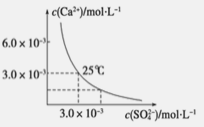
A.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B 溶液中析出CaSO4沉淀,溶液中c(Ca2+ )、c(SO 42-)都变小
C.溶液中无沉淀析出,溶液中c(Ca2+ )、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是 ( )
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com