
下列离子方程式正确的是
| A.铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| B.铜溶于稀硝酸:3Cu+ 8H+ +2NO3-=3Cu2+ +2NO↑ + 4H2O |
| C.碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑ + H2O |
| D.稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |
B
解析试题分析:A项,铝、氢元素化合价升降总数不相等、电子得失不守恒,且两边电荷总数不相等,说明没有配平,正确的是2Al+2OH—+2H2O=2AlO2—+3H2↑,故A选项错误;B项,稀硝酸具有强氧化性,能溶解金属活动顺序表中氢后金属铜,生成硝酸铜、一氧化氮和水,硝酸、硝酸铜是易溶且易电离的化合物,应改写为离子形式,且符合电子、电荷、原子守恒原理,故B选项正确;C项,由于盐酸的酸性比碳酸强,碳酸镁与盐酸反应生成氯化镁、二氧化碳和水,碳酸镁是不易溶的化合物,应保留化学式,不能改写为碳酸根离子形式,HCl、MgCl2都是易溶且易电离的化合物,都应改写为离子形式,即MgCO3+2H+=Mg2++CO2↑+H2O,故C选项错误;D项,稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水,硫酸钡是难溶物,应保留化学式,不能漏写该离子反应,即2H++SO42—+Ba2++2OH—=BaSO4↓+2H2O,故D选项错误。
考点:考查离子方程式的书写,涉及反应是否符合客观事实、电子得失或原子个数是否守恒、是否漏写离子反应、生成物能否与过量反应物继续反应、化合物拆写是否正确等。


科目:高中化学 来源: 题型:单选题
下列反应的离子方程式书写正确的是:
| A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN- = Fe(SCN)3↓ |
| B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2= I2 + 2H2O |
| C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH- = Na2SiO3↓+H2O |
| D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3- + OH-+ Ba2+ = H2O + BaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列溶液中各组离子一定能够大量共存的是
| A.加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
| B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
C.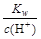 =0.1 mol·L-1的溶液:Na+、K+、SiO32—、NO3— =0.1 mol·L-1的溶液:Na+、K+、SiO32—、NO3— |
| D.通入足量SO2后的溶液:Na+、NH4+、ClO-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表对某些反应方程式的评价合理的是
| 编号 | 离子方程式或电极方程式 | 评价 | |
| A | Ca(ClO)2溶液中通入足量SO2 | Ca2++ClO-+SO2+H2O=CaSO4+Cl-+2H+ | 正确 |
| B | Ba(OH)2溶液中加入过量Al2(SO4)溶液 | 3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+Al(OH)3↓ | 正确 |
| C | 醋酸铵溶于水 | CH3COO-+NH4+ CH3COOH+NH3·H2O CH3COOH+NH3·H2O | 错误,阴阳离子水解相互促进,应该用“=”号 |
| D | 用惰性电极电解 CuCl2 和NaCl的混合溶液一段时间 | 阴极:Cu2++2e-=Cu 阳极:4OH—4e-=2H2O+O2 | 错误,只因为两级得失电子没配平 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式正确的是
| A.用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2 = NO+2NO↑+H2O |
B.NH4HCO3溶液与足量KOH浓溶液共热:NH+OH-  NH3↑+H2O NH3↑+H2O |
| C.铁溶于足量的稀硝酸,溶液变黄:3Fe+8H++2NO= 3Fe2++2NO↑+4H2O |
| D.NaHSO4溶液与NaOH溶液混合:OH-+H+= H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在水溶液中能大量共存的一组离子是
| A.H+、K+、Cl-、CO32- | B.Ba2+、Na+、SO42-、Cl- |
| C.ClO-、I-、K+、Mg2+ | D.Mg2+、K+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子能在溶液中大量共存的是
| A.Na+、NH4+、CO32-、Br- |
| B.Fe2+、H+、ClO-、Cl- |
| C.Al3+、Ca2+、HCO3-、SO42- |
| D.Fe3+、Cu2+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列用来表示物质变化的化学反应中正确的是
| A.表示中和热的热化学方程式:H++OH-=H2O △H=-57.3kJ·mol-1 |
| B.硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH-=NH3↑+H2O |
| C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
| D.足量酸性高锰酸钾溶液与双氧水反应的离子方程式:2MnO4-+5H218O2+6H+=2Mn2++518O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某强酸性溶液X可能含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是______,不能确定是否含有的离子(M)是______,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是______.
(2)写出反应②的离子方程式:______.
(3)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式______.
(4)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com