
| A. | 苯与溴水混合,振荡静置,溴水层褪色 | |
| B. | 乙烯通入酸性髙锰酸钾溶液中,溶液褪色 | |
| C. | 乙烯通入溴的四氛化碳溶液中,溶液褪色 | |
| D. | 甲烷与氯气混合光照,气体颜色变浅 |
分析 A、苯能萃取溴水中的溴;
B、高锰酸钾和乙烯发生了氧化反应;
C、乙烯的双键断裂,每个碳原子上结合一个溴原子生成二溴乙烷;
D、甲烷中的氢原子被氯原子所代替生成氯代物.
解答 解:A、苯能萃取溴水中的溴,所以水层颜色变浅,不是加成反应,故A错误;
B、乙烯使酸性高锰酸钾溶液褪色,是高锰酸钾和乙烯发生了氧化反应的结果,故B错误;
C、乙烯的双键断裂,每个碳原子上结合一个溴原子生成二溴乙烷,所以属于加成反应,故C正确;
D、甲烷和氯气混合光照一段时间后,甲烷中的氢原子被氯原子所代替生成氯代物,所以属于取代反应,故D错误;
故选C.
点评 本题主要考查了加成反应的判断,加成反应的条件是有机物中必须含有不饱和键.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:解答题
 ;该化合物的晶体类型离子晶体
;该化合物的晶体类型离子晶体查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 步骤(2)产物中残留的烯丙醇可用溴水检验 | |
| C. | 苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| D. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.25 mol•L-1•min-1 | B. | v(O2)=0.35mol•L-1•min-1 | ||
| C. | v(NO)=0.01 mol•L-1•s-1 | D. | v(H2O)=0.3 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(4)(5) | B. | (3)(1)(4)(2)(5) | C. | (5)(1)(3)(2)(4) | D. | (5)(4)(3)(2)(1) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
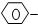 、-COOH 4种基团两两组合而成的有机物中,能跟NaOH溶液发生化学反应的有( )
、-COOH 4种基团两两组合而成的有机物中,能跟NaOH溶液发生化学反应的有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
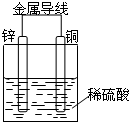
| A. | 锌为正极,发生氧化反应 | |
| B. | 铜为负极,铜片溶解 | |
| C. | 电子由铜片通过导线流向锌片 | |
| D. | 铜片上发生的电极反应:2 H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2、NH3的物质的量不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:2:3 | |
| C. | N2与H2物质的量之和是NH3的2倍 | |
| D. | 单位时间里每增加1mol N2,同时增加3mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
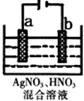 化学反应原理在生活和工业中应用广泛.
化学反应原理在生活和工业中应用广泛.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com