
| A、铁 | B、氯化钠 | C、酒精 | D、稀盐酸 |
科目:高中化学 来源: 题型:
| 实验序号 | 0.1032mol/L HCl溶液体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 26.53 | 25.00 |
| 3 | 27.85 | 25.00 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
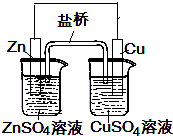
| A、锌是负极,发生氧化反应 |
| B、铜是正极,发生还原反应 |
| C、电流是从Zn流出经导线流入铜电极 |
| D、锌电极质量减少,铜电极质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
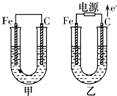 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将试纸一端浸入溶液,观察颜色变化 |
| B、先用水将pH试纸润湿后,再测定溶液的pH |
| C、将试纸一端在溶液中浸一段时间后,再与比色卡对照 |
| D、用洁净的玻璃棒蘸取被检液,滴在pH试纸中部,然后与比色卡对照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
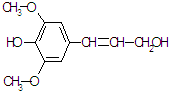 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关说法正确的是( )| A、芥子醇的分子式是C11H16O4 |
| B、芥子醇分子中所有碳原子不可能在同一平面 |
| C、芥子醇能与3mol溴水反应 |
| D、芥子醇能发生的反应类型有氧化、取代、加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com