
分析 已知物质的质量,根据n=$\frac{m}{M}$计算,H2PO4-的摩尔质量在数值上与式量相同,单位为g/mol.
解答 解:50.4g Ca(H2PO4)2•H2O晶体中,晶体的物质的量为:n=$\frac{m}{M}$=$\frac{50.4g}{252g/mol}$=0.2mol,则Ca(H2PO4)2的物质的量为0.2mol;
H2PO4-的摩尔质量在数值上与式量相同,单位为g/mol,则其摩尔质量为97g/mol.
故答案为:0.2mol;97g/mol.
点评 本题考查了物质的量的有关计算、摩尔质量的概念及单位,题目难度不大,侧重于考查学生对基础知识的把握及应用.


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
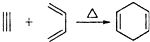 ,如果要合成
,如果要合成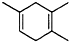 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 只有① | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com