
【题目】下列物质:①汽油、②四氯化碳、③酒精,可用作萃取碘水中碘的萃取剂是( )
A.①③B.②③C.①②D.①②③
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度(acidity grade),AG的定义为AG = lg[![]() ].室温下实验室中用0.01molL-1的氢氧化钠溶液滴定20.00mL 0.01molL-1的一元弱酸HA,滴定过程如图所示,下列叙述正确的是( )
].室温下实验室中用0.01molL-1的氢氧化钠溶液滴定20.00mL 0.01molL-1的一元弱酸HA,滴定过程如图所示,下列叙述正确的是( )

A. 室温下,弱酸HA的电离常数约为10-5
B. A点时加入氢氧化钠溶液的体积为20.00mL
C. 若B点为40mL,所得溶液中:c(OH-) = c(A-)+c(HA)+c(H+)
D. 反应过程中一定存在:0.01molL-1+c(OH-)=c(Na+)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是
A.CO2(SO2):饱和NaHCO3溶液B.FeCl2溶液(FeCl3):铜粉
C.Al2O3(SiO2):NaOH溶液D.Na2CO3(Na2SO4):BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)写出D在元素周期表中的位置为___________________ ,其三价阳离子的价层电子排布图为___________________ ;
(2)F元素位于元素周期表_________区,其基态原子有_________种能量不同的电子;
(3)第二周期中基态原子未成对电子数与E相同且电负性较大的元素为___________(写元素符号);
(4)E单质可作邻硝基苯酚或对硝基苯酚与H2加成的催化剂。邻硝基苯酚和对硝基苯酚在20![]() 水中的溶解度之比为0.39,其原因为___________________;
水中的溶解度之比为0.39,其原因为___________________;
(5)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。黄血盐的内界是_____(写出化学式),黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与黄血盐的配体互为等电子体的气态化合物,写出该气态化合物的电子式__________;
(6)E2+与Mg2+、O2﹣形成晶体的晶胞结构如下左图所示(E2+未画出),则该晶体的化学式为__.


(7)金属C、F晶体的晶胞结构如上图Ⅰ、Ⅱ(请先判断对应的图),金属F的晶胞中,若设该晶胞的密度为ag/cm3,阿伏加德罗常数的值为NA, F原子的摩尔质量为M g/mol,则表示F原子半径的计算式为______________pm(列出算式即可,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示。CH3-CH2=CHCH3可简写为![]() 。某有机物X的键线式为:
。某有机物X的键线式为: 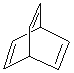
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。____________。
(2)Y在一定条件下发生聚合反应,写出其反应的化学方程式:_______________________。
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的二氯代物有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯并检验乙烯性质的装置如图。请回答有关问题:
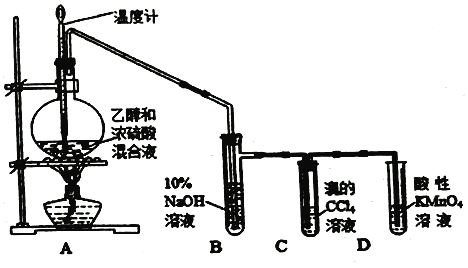
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是___________。
(2)烧瓶中产生乙烯的反应方程式为____________。
(3)反应开始后,可观察到C和D中共同的现象是___________;C中的反应类型为________、D中的反应类型为____________反应。
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是___________。
(5)10%的NaOH溶液起的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为______,晶体中原子间通过_____作用形成面心立方密堆积,其中M原子的配位数为______。
(2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
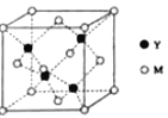
①该化合物的化学式为_______,已知晶胞参数a=0.542 nm,此晶体的密度为_______g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com