
| ���� | �� | �� | �� |
| ��ʼ��Ӧ��Ͷ���� | 2molH2��1molCO | 1molCH3OH | 2mol CH3OH |
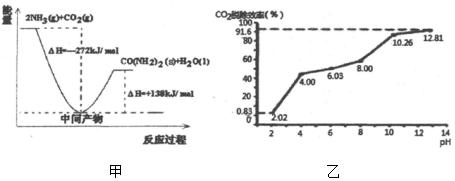
���� ��1����CO2�Ͱ����ϳ����أ���ͼ��֪����Ϊ��272kJ-138kJ��=134kJ��
��2���ٰ�ˮ���������е�CO2����̼����泥��ɷ�Ӧ���������д��ѧ����ʽ��
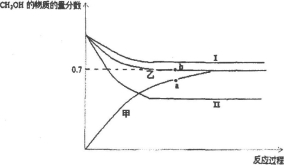
����ͼ��֪��pHΪ12.81�İ�ˮ��������ʱ�ѳ���CO2��Ч��Ϊ91.6%�����ѳ���CO2�����ʵ������Ϊx����$\frac{x}{12%}$=$\frac{0.052��1{0}^{3}L/h��0.5h}{22.4L/mol}$��91.6%��
��̼����鱗��ȶ��������ֽ⣻
��3�����ɱ������ݿ�֪��������ת��Ϊ�״�ʱ���ס�������ʼ����ͬ�����������ͼ������Iƽ��ʱ�״����������ʵ���Խ��ѹǿԽ��
��b��ʱ�״����ʵ�������Ϊ0.7����
CH3OH��g��?2H2��g��+CO��g��
��ʼ 1 0 0
ת�� x 2x x
ƽ�� 1-x 2x x
$\frac{1-x}{1-x+2x+x}$=0.7�����x=$\frac{1}{8}$mol��������ʵ��������������������
��� �⣺��1����ͼ��֪����Ϊ��272kJ-138kJ��=134kJ����CO2�Ͱ����ϳ������Ȼ�ѧ����ʽΪCO2��g��+2NH3��g��=CO��NH2��2��s��+H2O��l����H=-134kJ/mol��
�ʴ�Ϊ��CO2��g��+2NH3��g��=CO��NH2��2��s��+H2O��l����H=-134kJ/mol��
��2���ٰ�ˮ���������е�CO2����̼����泥���ѧ����ʽΪCO2+NH3��H2O=NH4HCO3��
�ʴ�Ϊ��CO2+NH3��H2O=NH4HCO3��
����ͼ��֪��pHΪ12.81�İ�ˮ��������ʱ�ѳ���CO2��Ч��Ϊ91.6%�����ѳ���CO2�����ʵ������Ϊx����CO2+NH3��H2O=NH4HCO3��֪��
��$\frac{x}{12%}$=$\frac{0.052��1{0}^{3}L/h��0.5h}{22.4L/mol}$��91.6%�����x=0.13mol��
�ʴ�Ϊ��0.13mol��
��ͨ��������¶����ߣ�CO2�ѳ�Ч����ߣ�������40��ʱ���ѳ�CO2Ч�ʽ��͵���Ҫԭ����̼����������ֽ�����CO2��
�ʴ�Ϊ��̼����������ֽ�����CO2��
��3�����ɱ������ݿ�֪��������ת��Ϊ�״�ʱ���ס�������ʼ����ͬ�����������ͼ������Iƽ��ʱ�״����������ܴ�������Ӧ��������I�����ʵ���Խ��ѹǿԽ��2H2��g��+CO��g��?CH3OH��g��Ϊ���������С�ķ�Ӧ��a��״������ʵ�������С���������ʵ�����Pa��Pb��
�ʴ�Ϊ��I������ƽ��ʱa��״������ʵ�������С���������ʵ�����
��b��ʱ�״����ʵ�������Ϊ0.7����
CH3OH��g��?2H2��g��+CO��g����H=+90kJ/mol
��ʼ 1 0 0
ת�� x 2x x
ƽ�� 1-x 2x x
$\frac{1-x}{1-x+2x+x}$=0.7�����x=$\frac{1}{8}$mol��
��֪b��ʱ��Ӧ���յ�����Ϊ$\frac{1}{8}$mol��90kJ/mol=11.25kJ��
�ʴ�Ϊ��11.25��
���� ���⿼����ۺϣ��漰�Ȼ�ѧ����ʽ����ѧƽ����㡢ƽ���ƶ��ȣ�Ϊ��Ƶ���㣬����ͼ�������ݡ���ѧ��Ӧԭ����Ӧ��Ϊ���Ĺؼ������ط�����Ӧ���������ۺϿ��飬�ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̿���л�ԭ�ԣ������������ζ�� | |
| B�� | ����������������ԣ���������ֽƯ�� | |
| C�� | Al2O3���кܸߵ��۵㣬���������������ռ������ | |
| D�� | FeCl3��Һ����Cu��Ӧ��������ʴ��ӡˢ��·�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
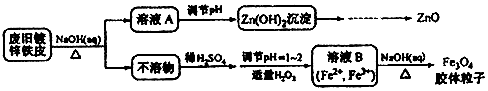
| A�� | ��NaOH��Һ�����Ͼɶ�п��Ƥ��������ȥ�����ۡ��ܽ��п�� | |
| B�� | ������ҺA��pH����Zn��OH��2�����������ˡ�ϴ�ӡ����ռ����Ƶ�ZnO | |
| C�� | ����ҺB�Ƶ�Fe3O4�������ӵĹ����У������ͨN2����ԭ���Ƿ�ֹFe2+������ | |
| D�� | Fe3O4�����������ü�ѹ���˷�ʵ�ֹ�Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
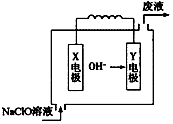 þ��һ����Ҫ�Ľ�����Դ���ڸ���������Ҫ�����ã�
þ��һ����Ҫ�Ľ�����Դ���ڸ���������Ҫ�����ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H2��0 | |
| B�� | BΪH2��O2�Ʊ�H2O2�Ĵ��� | |
| C�� | ��Ӧ�ٵ�����Ӧ�Ļ�ܴ����淴Ӧ�Ļ�� | |
| D�� | H2��g��+O2��g��?H2O2��1���ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeS2$\stackrel{O_{2}/����}{��}$SO2$\stackrel{H_{2}O_{2}��aq��}{��}$H2SO4 | |
| B�� | Cu2��OH��2CO3$\stackrel{H_{2}SO_{4}}{��}$CuSO4��aq��$\stackrel{Na}{��}$Cu | |
| C�� | MgCl2��aq��$\stackrel{��}{��}$MgCl2��s��$\stackrel{���}{��}$Mg | |
| D�� | 1mol•L-1HCl��aq��$\stackrel{MnO_{2}/��}{��}$Cl2$\stackrel{ʯ����}{��}$Ca��ClO��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �����÷�Ӧһ����Ҫ���Ȼ��ȼ������ | |
| B�� | E1�淴Ӧ�Ļ�ܣ�E2������Ӧ�Ļ�� | |
| C�� | �����ܼ�СE1��E2�������ı䷴Ӧ���ʱ� | |
| D�� | X��Y��Z��ʾ�ķ�Ӧ����֮��Ϊ2��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
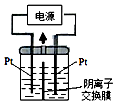 Ԫ�����ڱ��еڢ�A��Ԫ�صĵ��ʼ��仯�������;�㷺��
Ԫ�����ڱ��еڢ�A��Ԫ�صĵ��ʼ��仯�������;�㷺�� �������Ϻ�ɫ������ɫ���������ʣ���2�����ݵ���ʵ�������������ǻ���ʯ[Ca5��PO4��3OH]�ܽ�Ľ������մ���������ϣ���ø�������²����������ʣ������ȣ�ݣ�ʹ�ú�������ᱣ�����ݣ���Ϊ�����ӻ���ǻ���ʯ[Ca5��PO4��3OH]������Ӧ���ɷ���ʯ������ʯ���ǻ���ʯ���ֿܵ������ʴ���������ӷ���ʽ��ʾ��һ����Ca5��PO4��3OH��S��+F- ��aq��?Ca5��PO4��3 F��S��+OH-��aq������������ӻ������ƿ�ǻϸ�������ᣬ���������Ѿ��ձ�ʹ�ã�
�������Ϻ�ɫ������ɫ���������ʣ���2�����ݵ���ʵ�������������ǻ���ʯ[Ca5��PO4��3OH]�ܽ�Ľ������մ���������ϣ���ø�������²����������ʣ������ȣ�ݣ�ʹ�ú�������ᱣ�����ݣ���Ϊ�����ӻ���ǻ���ʯ[Ca5��PO4��3OH]������Ӧ���ɷ���ʯ������ʯ���ǻ���ʯ���ֿܵ������ʴ���������ӷ���ʽ��ʾ��һ����Ca5��PO4��3OH��S��+F- ��aq��?Ca5��PO4��3 F��S��+OH-��aq������������ӻ������ƿ�ǻϸ�������ᣬ���������Ѿ��ձ�ʹ�ã�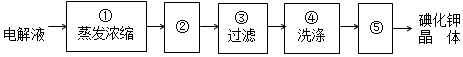
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com