
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯![]() 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
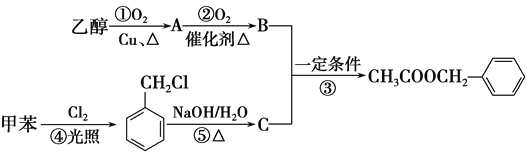
(1)B、C的结构简式分别为______________、________________。
(2)写出反应①、④的化学方程式:
①_____________________;④______________________。
(3)反应③、⑤的反应类型分别为③________,⑤____________。
(4)反应________(填序号)原子的理论利用率为100%,符合“绿色化学”的要求。
(5)乙酸苯甲酯的同分异构体中能与碳酸氢钠反应生成气体的有________种。
【答案】 CH3COOH ![]() 2CH3CH2OH+O2
2CH3CH2OH+O2![]() 2CH3CHO+2H2O 略 酯化(或取代)反应 水解(或取代)反应 ② 14
2CH3CHO+2H2O 略 酯化(或取代)反应 水解(或取代)反应 ② 14
【解析】由合成流程可以知道,乙醇在Cu或Ag催化作用下加热反应生成![]() ,
,![]() 继续被氧化为
继续被氧化为![]() ,甲苯光照下发生取代反应生成
,甲苯光照下发生取代反应生成![]() ,
,![]() 在碱性条件下水解生成C为
在碱性条件下水解生成C为![]() ,在一定条件下与
,在一定条件下与![]() 发生酯化反应生成
发生酯化反应生成![]() ,
,
(1)由以上分析可以知道B为![]() ,C为
,C为![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]() ;
;![]() ;
;
(2)反应①为乙醇催化氧化,生成乙醛和水,反应为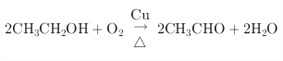 ,
,
反应④的方程式为![]()
![]()
![]()
![]() ,
,
因此,本题正确答案是: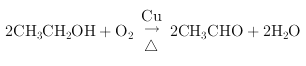 ;
; ![]()
![]()
![]()
![]() ;
;
(3)反应③的化学方程式![]() ,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
,为酯化反应或取代反应,⑤为氯代烃的水解反应,也为取代反应,
因此,本题正确答案是:酯化(或取代)反应;水解(或取代)反应。
(4)由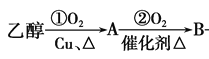 知反应②是乙醛的催化氧化反应,原子的理论利用率能达100%,符合“绿色化学”的要求,所以答案: ②。
知反应②是乙醛的催化氧化反应,原子的理论利用率能达100%,符合“绿色化学”的要求,所以答案: ②。
(5) 能与碳酸氢钠反应生成气体一定含有羧基,其乙酸苯甲酯的同分异构体有
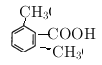 (6种)
(6种)![]() (3种)
(3种)![]() (2种)
(2种)
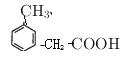 (3种)答案:14种。
(3种)答案:14种。


科目:高中化学 来源: 题型:
【题目】选择性催化还原法(SCR)烟气脱硝技术是一种成熟的NOx控制处理方法,主要反应如下:
①4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H1=akJ·mol-1
4N2(g)+6H2O(g) △H1=akJ·mol-1
②4NH3(g)+2NO2(g)+O2(g)![]() 3N2(g)+6H2O(g) △H2=bkJ·mol-1
3N2(g)+6H2O(g) △H2=bkJ·mol-1
副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H4=dkJ·mol-1
4NO(g)+6H2O(g) △H4=dkJ·mol-1
可以计算出反应2NO(g)+O2(g)![]() 2NO2(g)的△H为( )
2NO2(g)的△H为( )
A. (4b-3a+d)/4 B. (4a-3b+d)/4 C. (3b-4a+d)/4 D. (3a-4b+d)/4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A的结构简式如下:

(1)A的分子式是________。
(2)A在NaOH溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和![]() 四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
(3)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式__________________。
(4)写出B与碳酸氢钠反应的化学方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣氨基﹣3﹣氯苯甲酸(H)是重要的医药中间体,可以用来合成许多重要有机物,其制备流程图如下:

已知: 
回答下列问题:
(1)反应①的反应类型是________。
(2)写出反应②的化学反应方程式________。
(3)该流程未采用甲苯直接硝化的方法制备B,而是经由①②③三步反应制取B,目的是__________。
(4)E的结构简式为_______,对比D与H的结构简式,设计⑥~⑨四步反应实现转化的目的是_______。
(5)写出⑧的反应试剂和条件:_____。
(6)J是一种高分子化合物,写出反应⑩的化学反应方程式:_____。
(7)写出符合下列条件的B的所有同分异构体的结构简式__________。
a.苯环上只有两个取代基且互为邻位
b.既能发生银镜反应又能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,不正确的是( )
A.HCl═H++Cl﹣
B.NH3H2O═NH4++OH﹣
C.CaCl2=Ca2++2Cl﹣
D.CH3COOHCH3COO﹣+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银耳本身为淡黄色,某地出产一种雪耳,颜色洁白如雪,其制作过程如下:将银耳堆放在密封状况良好的塑料棚内,在棚的一端支一口锅,锅内放硫黄,加热使硫黄熔化并燃烧,两天左右雪耳就制成了。雪耳炖不烂,且对人体有害,制作雪耳利用的是( )
A.硫的还原性B.二氧化硫的漂白性C.二氧化硫的还原性D.硫的漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:______________________________________________。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的_________________。
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)==CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
键能/(kJ·mol-1) | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题:
①图1中曲线a到曲线b的措施是_________。

②已知CO中的C与O之间为叁键,其键能为x kJ/mol,则x=________。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为______________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为________。
(4)电解水蒸气和CO2产生合成气(H2
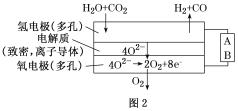
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温时,0.1mol·L-1的下列溶液①NH4Al(SO4)2 ②NH4Cl ③NH3·H2O ④CH3COONH4 中,c (NH4+)由大到小的顺序是:①>②>③>④
B. 0.1mol·L-1 NaHCO3溶液中,c(Na+)= 2c(CO32-)+ c(HCO3-)+c(H2CO3)
C. 常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)不相等
D. 常温时,0.3 mol·L-1HY溶液与0.3 mol·L-1NaOH溶液等体积混合后,溶液的pH=9,则混合溶液中c(H+) +c(HY)= 1×10-5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A. 60g丙醇中存在的共价键总数为10NA
B. 乙烯和聚乙烯的混合物共7g,完全燃烧所生成的CO2的分子数一定为0.5NA
C. 标准状况下,2.24LCHCl3分子中含有0.3NA个Cl
D. 一定温度下,1L 1mol·L-1的CH3COONa溶液含NA个CH3COO-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com