
【题目】下列化合物中,阴离子和阳离子的半径之比最小的是( )
A. CsF B. NaF C. LiI D. KCl
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
第二组 | NaOH | HCl | NaCl | Na2O | CO |
第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
每组分类均有错误,其错误的物质分别是______________(填化学式,下同)、________、________。
(2)胶体和溶液的本质区别是_____________________;
鉴别胶体和溶液所采用的方法是观察是否能发生________现象。
(3)下列3个反应,按要求填写相关量。
①2Na2O2+2H2O==4NaOH+O2↑反应中,每消耗1 mol Na2O2生成________g O2;
②2NaHCO3![]() Na2CO3+H2O+CO2↑反应中,每消耗168 g NaHCO3,标况下生成______L CO2;
Na2CO3+H2O+CO2↑反应中,每消耗168 g NaHCO3,标况下生成______L CO2;
③Cl2+H2O=HCl+HClO反应中,标况下每消耗22.4 L Cl2,转移________ mol电子。
(4)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
物质 | M | N | Q | P |
反应前质量(g) | 50] | 1 | 3 | 12 |
反应后质量(g) | X | 26 | 3 | 30 |
①该变化的基本反应类型是________反应;
②物质Q在反应中起的作用是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下现象与原电池反应无关的是( )
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比软铁芯(几乎是纯铁)容易生锈
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银质奖牌久置后表面变暗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阿伏加德罗常数的值为NA,下列说法正确的是( )
① 标准状况下,22.4 L CHCl3中含有的氧原子数目为3 NA
② 14 g乙烯和丙烯的混合物中总原子数为3 NA
③ 0.1 mol/L的氢氧化钠溶液中含钠离子数为0.1 NA
④ 1 mol NaHSO4晶体中含有的离子总数为3 NA
⑤ 标准状况下,NO和O2 各11.2 L混合,所得混合气体的分子总数为0.75 NA
⑥ 1 L 1 mol/L FeCl3完全水解生成NA个胶体粒子
⑦ 101 kPa、4℃时18 mL水和202 kPa、27℃时32 g O2所含分子数均为NA
⑧ 常温常压下,4.9 L的CO、O2、CO2混合气体含分子数共0.2 NA
A.只有①③⑦ B.除①⑧外 C.除⑥外 D.只有②⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 将0.4gNaOH和1.06gNa2CO3 混合并配成溶液,向溶液中滴加0.1mol·![]() 稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
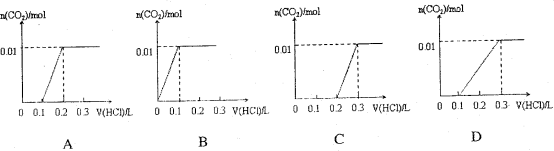
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。下列有关海水综合利用的说法不正确的是
A.从海水中提炼出的氘(含 HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题,
成为一条新的科学思路。HDO与 H2O化学性质相同
B.从海水中提取镁可以采用下列方法:
![]()
C.从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,已知该化合物中碘元素呈+3和+5两种价态,则这种化合物的化学式是 I4O9
D.除去粗盐中的 SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液![]() NaOH溶液
NaOH溶液![]() BaCl2溶液
BaCl2溶液![]() 过滤后加盐酸
过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)离子推断题:
有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量的BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,称量沉淀质量为6.99g;
②第二份逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如下图所示。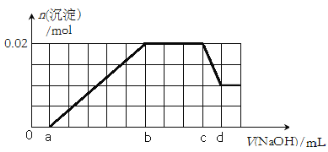
根据上述实验事实,回答以下问题:
(1)该溶液中一定不存在的阳离子有 ;
(2)在实验②中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为 ;NaOH溶液的浓度为 (用含字母c、d的代数式表示);
(3)确定原溶液一定含有Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为 (填数字,下同);
(4)原溶液中NO3-的浓度为c(NO3-),则c(NO3-)的取值范围为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物已略去):![]()
![]()
下列说法不正确的是
A. 若W是单质铁,则Z溶液可能是FeCl2溶液
B. 若W是盐酸,则X与Z可反应生成Y
C. 若X是FeCl3溶液,则W可以是Zn或Al
D. 若W是硝酸溶液, 则X与Z不能反应生成Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com