
| A、标准状况下,18g H2O含有10nA个电子 |
| B、等物质的量的H2和N2所含分子数均为NA |
| C、1 mol Cu与足量浓硫酸反应产生2NA个SO2分子 |
| D、1L0.1mol/L NH4Cl 溶液中含有NH4+数目为0.1NA |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 )代替两个NH3与铂配位,则生成的产物
)代替两个NH3与铂配位,则生成的产物 和氯化钠溶液反应制取
和氯化钠溶液反应制取  的离子反应方程式
的离子反应方程式 )及呋喃(
)及呋喃( )形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式
)形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①和③ |
| C、③和④ | D、①和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
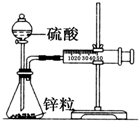 按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )
按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )| A、忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率0.01mol/(L?s) |
| B、忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率0.01mol/(L?s) |
| C、用锌粒来表示10s内该反应的速率为0.013g/s |
| D、用H2来表示10s内该反应的速率为0.0002mol/s |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度相同、体积相同的O2(g)和N2(g)分子数相同 |
| B、等温等压下,SO2气体与CO2气体的密度之比等于16:11 |
| C、温度和容积相同的两气罐中分别盛有5molO2(g)和2mol N2(g),两容积中的压强之比等于5:2 |
| D、等温等压条件下,5molO2(g)和2molH2(g)的体积之比等于5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol?L -1的NaClO溶液中含有ClO-的数目为NA |
| B、常温常压下,分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| C、标准状况下,11.2 L CH3CH2OH 中含有的氢原子数目为3NA |
| D、室温下,1L pH=13的Ba(OH)2溶液中,OH-离子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
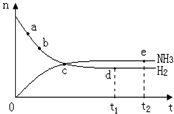 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:| 催化剂 |
| 高温高压 |
| A、点a的正反应速率比b点的大 |
| B、反应达到平衡时,v(N2)正=2v(NH3)逆 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点值大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、仅有①② | B、仅有①③④⑤ |
| C、仅有①③⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、砷的+3价化合物的毒性强于+5价化合物 |
| B、砷原子最外层有3个电子 |
| C、砷化氢(AsH3)比NH3稳定 |
| D、砷酸(H3AsO4)的酸性强于磷酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com