
【题目】将H2和CO以![]() =2的方式充入1 L的恒容密闭容器中,一定条件下发生反应:4H2(g)+2CO(g)
=2的方式充入1 L的恒容密闭容器中,一定条件下发生反应:4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g),测得CO的平衡转化率随温度、压强变化关系如图所示。下列说法正确的是
CH3OCH3(g)+H2O(g),测得CO的平衡转化率随温度、压强变化关系如图所示。下列说法正确的是
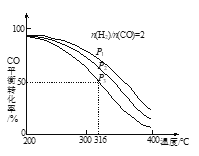
A.该反应的△H<0
B.压强大小:P1<P2<P3
C.在316℃时,该反应的平衡常数为0.25
D.若在P3和316℃时,起始时![]() =3,则达到平衡时,CO转化率大于50%
=3,则达到平衡时,CO转化率大于50%
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】某研究小组以有机物A为原料,合成抗癌药——拉帕替尼的中间体H的具体路线如下:
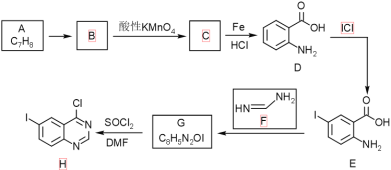
已知:①![]()
②![]()
回答下列问题:
(1)C的名称为________________。D中所含官能团的名称为________________。G的结构简式为________________。
(2)B→C的反应类型为________________。
(3)A分子中共面原子数最多为___________。
(4)A→B的化学方程式为____________________________________________。
(5)碳原子上连有4个不同原子或基团时,该碳原子为手性碳原子。写出D与足量H2反应后产物的结构简式,并用星号(*)标出其中的手性碳原子_________________。
(6)C有多种同分异构体,其中满足下列条件的同分异构体共有_______种。
①分子中含有苯环;②分子中含有-NO2(不考虑-O-NO2);③能发生银镜反应
其中核磁共振氢谱有3组峰,并且峰面积之比为1:2:2的有机物结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是合成一种天然茋类化合物的重要中间体,其合成路线如下:
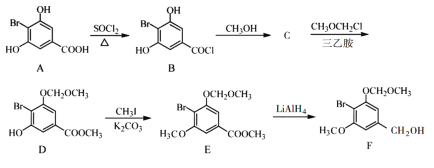
(1)A中含氧官能团的名称为_________。
(2)A→B的反应类型为________。
(3)写出B→C的化学反应方程式:________
(4)C→D的反应中有副产物X(分子式为C12H15O6Br)生成,写出X的结构简式:________。
(5)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________。
①能与FeCl3溶液发生显色反应;
②碱性水解后酸化,含苯环的产物分子中不同化学环境的氢原子数目比为1∶1。
(6)已知: (R表示烃基,R'和R"表示烃基或氢)
(R表示烃基,R'和R"表示烃基或氢)
写出以![]() 和CH3CH2CH2OH为原料制备
和CH3CH2CH2OH为原料制备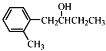 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)__________。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙烯的球棍模型为![]()
B.CH2=CH—CH3分子中,最多有7个原子共面
C.用溴水或酸性KMnO4溶液可以区分甲烷和乙烯,也可以除去甲烷中的乙烯杂质得到纯净甲烷
D.C2H4和SO2都能使溴水褪色,又能使酸性KMnO4溶液褪色,并且化学反应原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向KI溶液中滴入少量新制氯水和四氯化碳,振荡、静置,溶液下层呈紫红色 | I的还原性强于Cl |
B | 向无水乙醇中加入浓H2SO4,加热,将产生的气体通入酸性KMnO4溶液,紫红色褪去 | 该气体一定是乙烯 |
C | 测定Na2CO3和Na2SiO3溶液的pH,后者pH比前者的大 | C的非金属性比Si强 |
D | 向1-溴丙烷中加入KOH溶液,加热几分钟,冷却后再加入AgNO3溶液,无淡黄色沉淀生成 | 1-溴丙烷没有水解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式如图所示,下列说法不正确的是( )
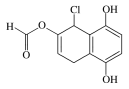
A.能发生银镜发应
B.能与FeCl3溶液发生显色反应
C.1 mol该物质最多可与4 mol NaOH反应
D.与NaHCO3、Na2CO3溶液均能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱除烟气中的氮氧化物(主要是指NO和NO2)可以净化空气、改善环境,是环境保护的主要课题。
(1)次氯酸盐氧化法。次氯酸盐脱除NO的主要过程如下:
i. NO+HClO=NO2+HCl
ii. NO+NO2+H2O![]() 2HNO2
2HNO2
iii. HClO+HNO2=HNO3+HCl
①下列分析正确的是______(填字母)。
A.烟气中含有的少量O2能提高NO的脱除率
B.NO2单独存在时不能被脱除
C.脱除过程中,次氯酸盐溶液的pH下降
②研究不同温度下Ca(ClO)2溶液对NO脱除率的影响,结果如图1所示
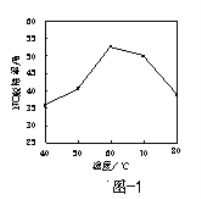
脱除过程中往往有Cl2产生,原因是______(用离子方程式表示);60~80℃NO脱除率下降的原因是______。
(2)尿素[CO(NH2)2]还原法。NO和NO2以物质的量之比1﹕1与CO(NH2)2反应生成无毒气体的化学方程式为______。
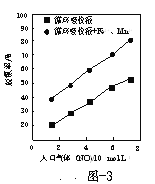
(3)脱氮菌净化法。利用脱氮菌可净化低浓度NO烟气,当烟气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如题16图2、题16图3所示。
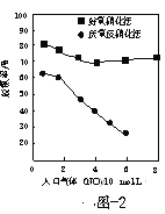
①由题图2知,当废气中的NO含量增加时,提高脱氮效率宜选用的方法是______。
②题图3中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是临床常用的镇静、麻醉药物,其合成路线流程图如下:
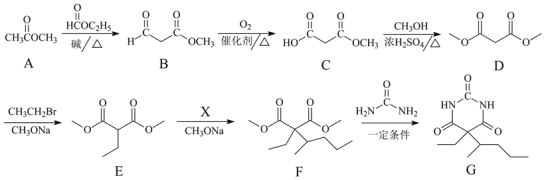
(1)B中的含氧官能团名称为______和______。
(2)D→E的反应类型为______。
(3)X的分子式为C5H11Br,写出X的结构简式:______。
(4)F→G的转化过程中,还有可能生成一种高分子副产物Y,Y的结构简式为______。
(5)写出同时满足下列条件的G的一种同分异构体的结构简式:______。
①分子中含有苯环,能与FeCl3溶液发生显色反应
②分子中只有4种不同化学环境的氢
(6)写出以CH2BrCH2CH2Br、CH3OH和CH3ONa为原料制备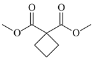 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应: PCl5(g) ![]() Cl2(g)+PCl3(g)经一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
Cl2(g)+PCl3(g)经一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
反应时间/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
(1)能表明该反应达到平衡状态的是________(填序号);
A.生成1molPCl3的同时生成1molPCl5 B.混合气体的平均相对分子质量不变
C.PCl5、Cl2、PCl3三者的浓度比值1:1:1 D.混合气体的密度不变
(2)上述温度下,达到平衡时,PCl5的转化率为____;该反应的平衡常数K= ___。
(3)反应在前50 s内的平均速率为v(PCl3)=_____。
(4)保持其他条件不变,若升高温度,反应重新达到平衡,平衡时c(PCl3)=0.11moI·L-l,则正反应的ΔH__0(填“>”或“<”)。
(5)相同温度下,若起始时向容器中充入1.0 molPCl5、0.20mol PCl3和0.20 mol Cl2,则反应达到平衡前v(正) __ v(逆)(填“>”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com