
| A、将氯化铝溶液加热,蒸干后得到无水氯化铝固体 |
| B、向Fe(OH)3胶体通电,发现胶体向正极移动,根据电场的作用,我们可以得出,Fe(OH)3带负电 |
| C、23Na37Cl中的质子数和中子数之比7:8 |
| D、硝酸铝溶液中滴加少量的氢氧化钠生成Al(OH)3 |


科目:高中化学 来源: 题型:
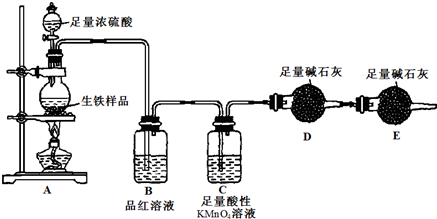
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸钠溶液显碱性 |
| B、常温时,0.1 mol?L-1乙酸溶液的pH约为3 |
| C、10mL 1mol?L-1乙酸溶液与10mL1mol?L-1的NaOH溶液恰好完全反应 |
| D、在相同温度下,同物质的量浓度的乙酸溶液的导电性比甲酸(为弱酸)溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在使用过程中,电池负极区溶液pH增大 |
| B、在使用过程中,电流由Ag2O极经外电路流向Zn极 |
| C、在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D、外电路中每通过0.2mol电子,正极的质量理论上减小33.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、HClO、AlCl3 |
| B、NaOH、NH3 |
| C、LiOH、PCl3 |
| D、HCN、BF3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
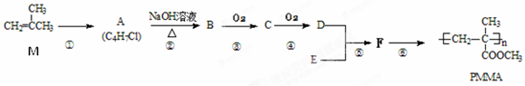
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com