

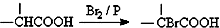
 ��
�� ��
��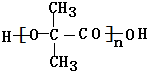 +��n-1��H2O���÷�Ӧ�������۷�Ӧ���Ӧ���ͣ���
+��n-1��H2O���÷�Ӧ�������۷�Ӧ���Ӧ���ͣ��� ���� C�IJ����Ͷ�=$\frac{8��2+2-8}{2}$=5��C����̼�����Ʒ�Ӧ��˵��C�к����Ȼ�������������������Һ�巴Ӧֻ������2�ַе㲻ͬ��һ��������廯�����C�ṹ��ʽΪ ��Aˮ����������ʹ���C�����ᣬ��B�Ǵ���B����������������D��D�ܷ�����Ϣ�ڵķ�Ӧ��AΪ����A�к���2��Oԭ�ӣ���A��Է�������=$\frac{16��2}{16.7%}$��192��B��Է�������=192+18-8��12-8��1-16��2=74��BΪһԪ��ʱ��̼ԭ�Ӹ���=$\frac{74-16-2}{14}$=4���������⣬����B�к���4��̼ԭ�ӣ�B��������������������D��D����ȡ����Ӧ����E��E������ȥ��Ӧ����F��F�������۷�Ӧ����G��G�Ĵֲ����У�������Ԫ��״����������H�������H�ĺ˴Ź�������ֻ��һ���壬��G�ṹ��ʽΪ
��Aˮ����������ʹ���C�����ᣬ��B�Ǵ���B����������������D��D�ܷ�����Ϣ�ڵķ�Ӧ��AΪ����A�к���2��Oԭ�ӣ���A��Է�������=$\frac{16��2}{16.7%}$��192��B��Է�������=192+18-8��12-8��1-16��2=74��BΪһԪ��ʱ��̼ԭ�Ӹ���=$\frac{74-16-2}{14}$=4���������⣬����B�к���4��̼ԭ�ӣ�B��������������������D��D����ȡ����Ӧ����E��E������ȥ��Ӧ����F��F�������۷�Ӧ����G��G�Ĵֲ����У�������Ԫ��״����������H�������H�ĺ˴Ź�������ֻ��һ���壬��G�ṹ��ʽΪ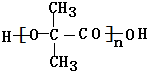 ��H�ṹ��ʽΪ
��H�ṹ��ʽΪ ����B�ṹ��ʽΪ��CH3��2CHCH2OH��D�ṹ��ʽΪ��CH3��2CHCOOH��E�ṹ��ʽΪ��CH3��2CBrCOOH��F�ṹ��ʽΪ��CH3��2C��OH��COOH��A�ṹ��ʽΪ
����B�ṹ��ʽΪ��CH3��2CHCH2OH��D�ṹ��ʽΪ��CH3��2CHCOOH��E�ṹ��ʽΪ��CH3��2CBrCOOH��F�ṹ��ʽΪ��CH3��2C��OH��COOH��A�ṹ��ʽΪ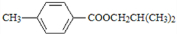 ���ݴ˷������
���ݴ˷������
��� �⣺C�IJ����Ͷ�=$\frac{8��2+2-8}{2}$=5��C����̼�����Ʒ�Ӧ��˵��C�к����Ȼ�������������������Һ�巴Ӧֻ������2�ַе㲻ͬ��һ��������廯�����C�ṹ��ʽΪ ��Aˮ����������ʹ���C�����ᣬ��B�Ǵ���B����������������D��D�ܷ�����Ϣ�ڵķ�Ӧ��AΪ����A�к���2��Oԭ�ӣ���A��Է�������=$\frac{16��2}{16.7%}$��192��B��Է�������=192+18-8��12-8��1-16��2=74��BΪһԪ��ʱ��̼ԭ�Ӹ���=$\frac{74-16-2}{14}$=4���������⣬����B�к���4��̼ԭ�ӣ�B��������������������D��D����ȡ����Ӧ����E��E������ȥ��Ӧ����F��F�������۷�Ӧ����G��G�Ĵֲ����У�������Ԫ��״����������H�������H�ĺ˴Ź�������ֻ��һ���壬��G�ṹ��ʽΪ
��Aˮ����������ʹ���C�����ᣬ��B�Ǵ���B����������������D��D�ܷ�����Ϣ�ڵķ�Ӧ��AΪ����A�к���2��Oԭ�ӣ���A��Է�������=$\frac{16��2}{16.7%}$��192��B��Է�������=192+18-8��12-8��1-16��2=74��BΪһԪ��ʱ��̼ԭ�Ӹ���=$\frac{74-16-2}{14}$=4���������⣬����B�к���4��̼ԭ�ӣ�B��������������������D��D����ȡ����Ӧ����E��E������ȥ��Ӧ����F��F�������۷�Ӧ����G��G�Ĵֲ����У�������Ԫ��״����������H�������H�ĺ˴Ź�������ֻ��һ���壬��G�ṹ��ʽΪ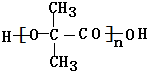 ��H�ṹ��ʽΪ
��H�ṹ��ʽΪ ����B�ṹ��ʽΪ��CH3��2CHCH2OH��D�ṹ��ʽΪ��CH3��2CHCOOH��E�ṹ��ʽΪ��CH3��2CBrCOOH��F�ṹ��ʽΪ��CH3��2C��OH��COOH��A�ṹ��ʽΪ
����B�ṹ��ʽΪ��CH3��2CHCH2OH��D�ṹ��ʽΪ��CH3��2CHCOOH��E�ṹ��ʽΪ��CH3��2CBrCOOH��F�ṹ��ʽΪ��CH3��2C��OH��COOH��A�ṹ��ʽΪ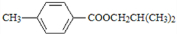 ��
��
��1��ͨ�����Ϸ���֪��A����ʽΪC12H16O2���ʴ�Ϊ��C12H16O2��
��2��C�ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��CΪ ��C��ͬ���칹���ܷ���������Ӧ���ܷ���ˮ�ⷴӦ��˵������������ȩ����Ϊ��������ȡ����ΪHCOO-��-CH3�����ڼ�����֣�ȡ����ΪHCOOCH2-����һ�֣����Է�����������4�֣��ʴ�Ϊ��4��
��C��ͬ���칹���ܷ���������Ӧ���ܷ���ˮ�ⷴӦ��˵������������ȩ����Ϊ��������ȡ����ΪHCOO-��-CH3�����ڼ�����֣�ȡ����ΪHCOOCH2-����һ�֣����Է�����������4�֣��ʴ�Ϊ��4��
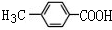
��4����G�Ĵֲ����У�������Ԫ��״����������H�������H�ĺ˴Ź�������ֻ��һ���壬��H�ṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
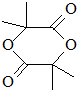
��5��G�ṹ��ʽΪ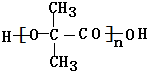 ��F�ṹ��ʽΪ��CH3��2C��OH��COOH��F�������۷�Ӧ����G����Ӧ���������۷�Ӧ��
��F�ṹ��ʽΪ��CH3��2C��OH��COOH��F�������۷�Ӧ����G����Ӧ���������۷�Ӧ��
��Ӧ����ʽΪn��CH3��2C��OH��COOH$\stackrel{һ��������}{��}$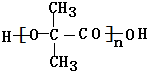 +��n-1��H2O��
+��n-1��H2O��
�ʴ�Ϊ��n��CH3��2C��OH��COOH$\stackrel{һ��������}{��}$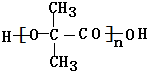 +��n-1��H2O�����۷�Ӧ��
+��n-1��H2O�����۷�Ӧ��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ���������ȷ�ж�A�ṹ��ʽ�ǽⱾ��ؼ���ע���������Ϣ����֪ʶǨ�Ʒ��������ƶϣ���Ҫѧ���������ջ���֪ʶ��������ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
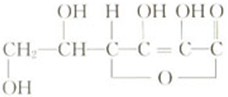 ά����C�Ľṹʽ���£�
ά����C�Ľṹʽ���£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7.8 g Na2O2������ˮ��Ӧת�Ƶĵ�����Ϊ0.2NA | |
| B�� | 5.6 g���������ᷴӦʧȥ�ĵ�����һ��Ϊ0.3NA | |
| C�� | ���³�ѹ�£�1 mol CH4�к��е���ԭ����Ϊ4NA | |
| D�� | 12.0 g���ڵ�NaHSO4�к���0.1NA��Na+��0.1NA��H+��0.1NA��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� |
| A | ��ǿ�������ȡ������ | ��������Һ����ȡ���� |
| B | ��Ӧ��Ũ��Խ��Ӧ����Խ�� | �����£���ͬ����Ƭ�зֱ����������Ũ��ϡ���ᣬŨ��������Ƭ���ܽ��� |
| C | �ṹ��������Ƶ����ʣ��е�����Է���������������� | NH3�е����PH3 |
| D | �ܽ��С�����������ܽ�ȸ�С������ת�� | ����ʯ��ˮ��ͨ��CO2��ʯ��ˮ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij������ˮ�к�����̬�ȣ�ͨ������ʵ��ⶨ��Ũ�ȣ�
ij������ˮ�к�����̬�ȣ�ͨ������ʵ��ⶨ��Ũ�ȣ��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com