
【题目】T℃时,在容积均为0.5L的两个密闭容器中发生:2A(g)+B(g)2C(g)△H=﹣Q kJ/mol (Q>0),6min后,容器①中反应达平衡,有关数据如下表,下列叙述中正确的是
容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 0.75QkJ |
② | 0.4 | 0.2 | 1.6 | |
A. 0-6min,v(A)=0.25mol/(L·min)
B. ②中达平衡时放出的热量为0.05QkJ
C. 其他条件不变,若容器②保持绝热恒容,则达到平衡时C的体积分数小于2/3
D. 若①达平衡后,再通入1molA与0.5molB,再达平衡时A的转化率增大
【答案】D
【解析】容器①中参加反应的A的物质的量=2mol×0.75QkJ/QkJ=1.5mol,浓度是1.5mol÷0.5L=3.0mol/L,则0~6min,v(A)=3.0mol/L÷6min=0.5mol/(L·min),A错误;B、根据以上分析可知
2A(g)+B(g)![]() 2C(g)
2C(g)
起始(mol):2 1 0
转化(mol):1.5 0.75 1.5
平衡(mol):0.5 0.25 1.5
恒温恒容下,②中完全转化到方程式左边可以得到2molA、1molB,容器①、②反应为完全等效平衡,平衡时各组分的物质的量相等,②中吸收的热量为(0.25-0.2)mol×Q kJ/mol=0.05Q kJ,B错误;C.平衡时①、②中C的体积分数为1.5mol/(0.5+0.25+1.5)mol=2/3,其他条件不变,若容器②保持恒容绝热,随反应进行,温度降低,反应向生成C的方向移动,生成2molC时,混合气体减小1mol,则达到平衡时C的体积分数大于2/3,C错误;D. 若①达平衡后,再通入1molA与0.5molB,相当于增大压强平衡向正反应方向进行,再达平衡时A的转化率增大,D正确,答案选D。


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】某工业废料中主要含有Al2O3、Co2O3CoO、少量Fe3O4等金属氧化物(Co2O3CoO不与强碱反应).实验室科技人员欲将之分离并制备相关物质,设计流程如下: 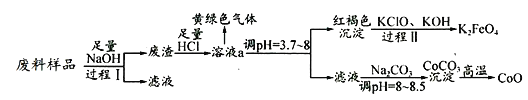
(1)过程Ⅰ中的操作名称是__,写出过程Ⅰ发生反应的化学方程式____________.
(2)溶液a中含有金属离子有 _________________.
(3)溶液a中逸出的黄绿色气体是氯气,下列说法不正确的是_________.
①氯气是有漂白性的酸性气体
②液氯和氯水均为液体,且都含有氯分子
③将氯气通入碱液时,氯气既是氧化剂,又是还原剂
④次氯酸见光易分解,说明次氯酸是弱酸
⑤向氯水中滴硝酸银溶液,有白色沉淀生成,说明氯水中含Cl-
(4)写出过程Ⅱ发生反应的离子方程式:_______________________________.
高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阳极反应式为___________________________________.
(5)Co可以形成CoC2O42H2O(M为183g/mol),5.49g该晶体在空气中加热,在不同温度下分别得到一种固体物质,其质量如表:
温度范围(℃) | 固体质量(g) |
150﹣210 | 4.41 |
290﹣320 | 2.41 |
890﹣920 | 2.25 |
经测定,210℃~290℃过程中,产生的气体只有CO2,则此过程发生的化学反应方程式为:______________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. υ(A)=0.5mol/(L·s) B. υ(B)=0.3mol/(L· s) C. υ(C)=0.8mol/(L·s) D. υ(D)=1mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于0.1mol/L Na2CO3溶液的叙述错误的是( )
A.0.5 L该溶液中钠离子的物质的量浓度为0.1 mol/L
B.1 L该溶液中含有Na2CO3的质量为10.6 g
C.从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.01 mol/L
D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯化钠、氯化铝、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是(
A. KSCNB. NaOHC. HClD. BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 室温下,1L pH=3的NH4Cl溶液中,由水电离的H+数目为10-11NA
B. 0.1mol Na2O2与足量的潮湿的CO2反应转移的电子数为0.1NA
C. 标准状况下,6.0gNO和2.24L O2混合,所得气体的分子数目为0.2NA
D. pH=2的NaHSO4溶液中的SO42-的数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A | B | C | D | |
实 | 用CCl4提取 | 除去乙醇中的苯酚 | 从KI和I2的固体 | 配制100mL 0.1000 |
装 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A. 加入盐酸以除去硫酸钠中的少量碳酸钠杂质
B. 配制溶液定容时,用胶头滴管滴加蒸馏水至溶液凹液面最低点与刻度线相切
C. 用分液漏斗分离液体时,先放出下层液体后,再放出上层液体
D. 萃取时,将酒精和碘化钾溶液放入分液漏斗中静置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于以下装置的描述正确的是( )

A. 乙装置工作时, CuSO4溶液中可能出现K+,ZnSO4溶液中可能出现Cl-
B. 甲、乙的电路中各转移 1 mol电子时,溶液中各生成1 mol ZnSO4
C. 取出盐桥,灯泡仍可发光
D. 甲、乙两装置中的总反应式不可能相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com