解答:
解(1)分别取0.1mol钠、镁、铝与足量盐酸反应,则:
2Na+2HCl=2NaCl+H
2↑、Mg+HCl=MgCl
2+H
2↑、2Al+6HCl=AlCl
3+3H
2↑,
0.1mol 0.05mol 0.1mol 0.1mol 0.1mol 0.15mol
故在相同条件下产生氢气的体积比=0.05mol:0.1mol:0.15mol=1:2:3,
故答案为:1:2:3;
(2)设wg钠、镁、铝与足量盐酸反应,则:
2Na+2HCl=2NaCl+H
2↑、
46g 1mol
Wg x
故x=
=
mol
Mg+2HCl=MgCl
2+H
2↑
24g 1mol
Wg y
故y=
=
mol
2Al+6HCl=AlCl
3+3H
2↑,
54g 3mol
Wg z
故Z=
=
mol
故wg钠、镁、铝与足量盐酸反应,相同条件下产生氢气的体积比=
mol:
mol:
mol=
:
:
=36:69:92;
故答案为:36:69:92;
(3)产生相同物质的量的氢气,设氢气为3mol,则:
2Na+2HCl=2NaCl+H
2↑、Mg+HCl=MgCl
2+H
2↑、2Al+6HCl=AlCl
3+3H
2↑,
6mol 3mol 3mol 3mol 2mol 3mol
故所需钠、镁、铝的物质的量之比=6mol:3mol:2mol=6:3:2,
故答案为:6:3:2;
(4)依据(3)计算结果,若产生相同体积(同温同压下)的氢气,所需钠、镁、铝的质量之比是=6×23:3×24:2×27=23:12:9
故答案为:23:12:9;
(5)在100ml 0.1mol/L的Al
2(SO
4)
3溶液中加入0.5mol/L的NaOH溶液,如硫酸铝完全生成Al(OH)
3,则沉淀的质量为:0.1L×0.1mol/L×2×78g/mol=1.56g,
而此时为1.17g,说明硫酸铝并没有完全转化为Al(OH)
3,此时n(Al(OH)
3)=
=0.015mol,NaOH可能有两种情况,一是不足,二是使Al(OH)
3部分溶解,
当NaOH不足时,
Al
3++3OH
-=Al(OH)
3↓
3mol 1mol
x 0.015mol
则x=0.045mol,
V
1(NaOH溶液)=
=0.09L=90mL,
如使Al(OH)
3部分溶解,
①Al
3++3OH
-=Al(OH)
3↓
0.02mol 0.06mol
②Al(OH)
3+OH
-=AlO
2-+2H
2O
1mol 1mol
(0.02-0.015)mol (0.02-0.015)mol=0.005mol
两步反应共需要0.06mol+0.005mol=0.065mol,
V
2(NaOH溶液)=
=0.13L=130mL,
故答案为:130 或.90 mL;



 阅读快车系列答案
阅读快车系列答案 (1)将锌片和银片用导线相连浸入稀硫酸中组成原电池.该电池中负极发生
(1)将锌片和银片用导线相连浸入稀硫酸中组成原电池.该电池中负极发生 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: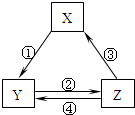 下表各组物质之间通过一步反应可以实现如图所示转化关系的是( )
下表各组物质之间通过一步反应可以实现如图所示转化关系的是( )