
已知X、Y、M、N之间的转化关系如图所示。下列说法正确的是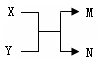
| A.若X为Fe,N为氢气,则Y一定为酸 |
| B.若X、N为化合物,Y为水,则M一定是气体单质 |
| C.若X、Y、M、N均为化合物,该反应一定属于复分解反应 |
| D.若X、Y、M、N均为10电子微粒,且M是工业生产HNO3的一种原料气,则N常温下一定呈液态 |
科目:高中化学 来源: 题型:单选题
下列反应中既能与强酸又能与强碱溶液反应的一组物质是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
| A.只有① | B.只有② | C.只有③ | D.①、②、③、④均可 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g,则原硫酸的物质的量浓度为 ( )。
| A.1 mol·L-1 | B.1.5 mol·L-1 |
| C.2 mol·L-1 | D.2.5 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
把一块镁铝合金投入到20 mL 1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法中正确的是( )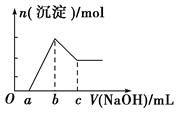
| A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中 |
| B.c值越大,合金中Al的含量越高 |
| C.b值越大,合金中Mg的含量越高 |
| D.假设c=25,整个反应过程中,主要发生了5个离子反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案: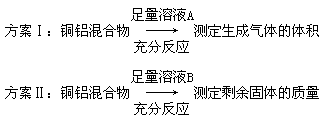
下列有关判断中不正确的是( )
| A.溶液A和B均可以是盐酸或NaOH溶液 |
| B.溶液A和B均可以选用稀硝酸 |
| C.若溶液B选用浓硝酸,则测得铜的质量分数偏小 |
| D.实验室方案Ⅱ更便于实施 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)。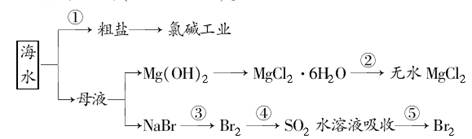
下列有关说法不正确的是( )
| A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能的过程 |
| B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| C.在过程③⑤中溴元素均被氧化 |
| D.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入化学药品的顺序为:Na2CO3溶液―→NaOH溶液―→BaCl2溶液―→过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
海水中含有氯化镁,是镁的重要来源之一。从海水中提取镁,可按照以下步骤进行:
①把贝壳制成石灰乳
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤、干燥产物
④将所得的产物熔融后电解。
关于提取镁,下列说法不正确的是( )
| A.此法的优点之一是原料来源丰富 |
| B.进行①、②、③步操作的目的是从海水中提取氯化镁 |
| C.第④步电解时会产生氯气 |
| D.以上提取镁的过程中涉及的反应有分解反应、化合反应、复分解反应和置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com