
ЁОЬтФПЁПЁОЛЏбЇЁЊбЁаоЃКгаЛњЛЏбЇЛљДЁЁП
ОлЗМжЌЃЈPAPЃЉЪЧЗжзгжїСДЩЯДјгаБНЛЗКЭжЌЛљЕФЬижжЙЄГЬЫмСЯЃЌдкКНПеКНЬьЕШСьгђОпгаЙуЗКгІгУЁЃЯТЭМЪЧРћгУввѕЃБћЫсЃЈCH2COCH2CH2COOHЃЉКЯГЩОлЗМжЌEЕФТЗЯпЃК

вбжЊЃКI. ![]()
II. ![]() ЃЈRЁЂRЁфБэЪОЬўЛљЃЉ
ЃЈRЁЂRЁфБэЪОЬўЛљЃЉ
(1)ввѕЃБћЫсжаКЌгаЕФЙйФмЭХУћГЦЮЊ_____________ЁЃ
(2)BЕФЗжзгЪНЮЊ_________________ЃЌDЕФНсЙЙМђЪНЮЊ___________ЁЃ
(3)ЗДгІЂкЕФЛЏбЇЗДгІЗНГЬЪНЮЊ______________ЃЌЗДгІРраЭЮЊ_______________ЁЃ
(4)ЗДгІЂнЕФЛЏбЇЗДгІЗНГЬЪНЮЊ______________ЃЌЗДгІРраЭЮЊ_______________ЁЃ
(5)ЗћКЯЯТСаЬѕМўЕФCЕФЭЌЗжвьЙЙЬхга________жжЁЃ
a.ФмЗЂЩњвјОЕЗДгІ b.ФмгыNaHCO3ШмвКЗДгІ
c.ЗжзгжагаБНЛЗЃЌЮо![]() НсЙЙ
НсЙЙ
дкЩЯЪіЭЌЗжвьЙЙЬхжаЃЌгавЛжжБНЛЗЩЯгаСНИіШЁДњЛљЧвКЫДХЙВеёЧтЦзЭМга4зщЗхЕФЮяжЪЃЌаДГіИУЮяжЪгызуСПNaOHШмвКЙВШШЗДгІЕФЛЏбЇЗНГЬЪН_____________ЁЃ
ЁОД№АИЁПєЪЛљЁЂєШЛљC19H22O4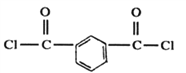
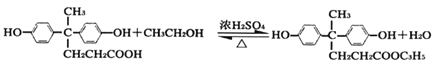 ѕЅЛЏЗДгІЃЈШЁДњЗДгІЃЉ
ѕЅЛЏЗДгІЃЈШЁДњЗДгІЃЉ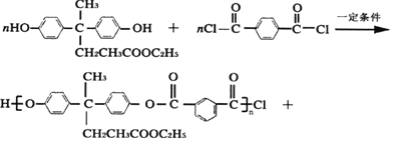 (2n- 1) HC1 ЫѕОлЗДгІ13
(2n- 1) HC1 ЫѕОлЗДгІ13![]()
ЁОНтЮіЁПгЩОлЗМЯуѕЅНсЙЙМђЪНжЊНсКЯAЕФЗжзгЪНжЊЃЌЗДгІЂйЮЊМгГЩЗДгІЃЌЧвЮЊЗгєЧЛљЕФЖдЮЛМгГЩЃЌдђAЮЊ ЃЌЗДгІЂкЮЊѕЅЛЏЗДгІЃЌдђBЮЊ
ЃЌЗДгІЂкЮЊѕЅЛЏЗДгІЃЌдђBЮЊ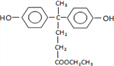 ЃЌЗДгІЂлЮЊбѕЛЏЗДгІЃЌдђCЮЊ
ЃЌЗДгІЂлЮЊбѕЛЏЗДгІЃЌдђCЮЊ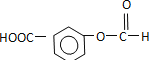 ЃЌЗДгІЂмЮЊШЁДњЗДгІЃЌдђDЮЊ
ЃЌЗДгІЂмЮЊШЁДњЗДгІЃЌдђDЮЊ![]() ЃЌЗДгІЂнЮЊЫѕОлЗДгІЃЌЩњГЩEЃЛ
ЃЌЗДгІЂнЮЊЫѕОлЗДгІЃЌЩњГЩEЃЛ
ЃЈ1ЃЉввѕЃБћЫсжаКЌгаЕФЙйФмЭХЪЧєЪЛљКЭєШЛљЃЛ
ЃЈ2ЃЉЭЈЙ§вдЩЯЗжЮіжЊЃЌBЮЊ ЃЌЦфЗжзгЪНЮЊC19H22O4ЃЌDНсЙЙМђЪНЮЊ
ЃЌЦфЗжзгЪНЮЊC19H22O4ЃЌDНсЙЙМђЪНЮЊ![]() ЃЛ
ЃЛ
(3)ЗДгІЂкЮЊ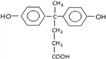 гыввДМЗЂЩњѕЅЛЏЗДгІЩњГЩ
гыввДМЗЂЩњѕЅЛЏЗДгІЩњГЩ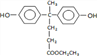 ЕФЛЏбЇЗДгІЗНГЬЪНЮЊ
ЕФЛЏбЇЗДгІЗНГЬЪНЮЊ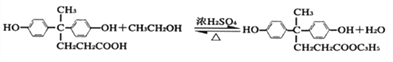 ЃЌЗДгІРраЭЮЊѕЅЛЏЗДгІЃЈЛђШЁДњЗДгІЃЉЃЛ
ЃЌЗДгІРраЭЮЊѕЅЛЏЗДгІЃЈЛђШЁДњЗДгІЃЉЃЛ
(4)ЗДгІЂнЮЊ КЭ
КЭ![]() ЗЂЩњЫѕОлЗДгІЩњГЩEЃЌЦфЛЏбЇЗДгІЗНГЬЪНЮЊ
ЗЂЩњЫѕОлЗДгІЩњГЩEЃЌЦфЛЏбЇЗДгІЗНГЬЪНЮЊ![]() ЃЌЗДгІРраЭЮЊЫѕОлЗДгІЃЛ
ЃЌЗДгІРраЭЮЊЫѕОлЗДгІЃЛ
ЃЈ5ЃЉCЮЊ ЃЌЗжзгЪНЮЊC8H6O4ЃЌCЕФЭЌЗжвьЙЙЗћКЯЯТСаЬѕМўЃКЂйФмЗЂЩњвјОЕЗДгІЫЕУїКЌгаШЉЛљЃЌЂкФмгыNaHCO3ШмвКЗДгІЫЕУїКЌгаєШЛљЃЌ
ЃЌЗжзгЪНЮЊC8H6O4ЃЌCЕФЭЌЗжвьЙЙЗћКЯЯТСаЬѕМўЃКЂйФмЗЂЩњвјОЕЗДгІЫЕУїКЌгаШЉЛљЃЌЂкФмгыNaHCO3ШмвКЗДгІЫЕУїКЌгаєШЛљЃЌ
ЂлЗжзгжагаБНЛЗЃЌЗжзгжаЮо![]() НсЙЙЃЌЦфЭЌЗжвьЙЙЬхжаКЌ-CHOЁЂ-COOHЁЂЗг-OHМАБНЛЗЃЌвЦЖЏШЁДњЛљЕФЮЛжУЃЌга4+4+2=10жжЃЌШєКЌHCOO-КЭ-COOHЃЌДцдкСкЁЂМфЁЂЖд3жжЃЌЙВга10+3=13жжЃЛдкЩЯЪіЭЌЗжвьЙЙЬхжаЃЌгавЛжжБНЛЗЩЯгаСНИіШЁДњЛљЧвКЫДХЙВеёЧтЦзЭМга4жжЗхЕФЮяжЪЫЕУїИУЮяжЪжаКЌга4жжЧтдзгЃЌЗћКЯЬѕМўЕФЭЌЗжвьЙЙЬхЮЊ
НсЙЙЃЌЦфЭЌЗжвьЙЙЬхжаКЌ-CHOЁЂ-COOHЁЂЗг-OHМАБНЛЗЃЌвЦЖЏШЁДњЛљЕФЮЛжУЃЌга4+4+2=10жжЃЌШєКЌHCOO-КЭ-COOHЃЌДцдкСкЁЂМфЁЂЖд3жжЃЌЙВга10+3=13жжЃЛдкЩЯЪіЭЌЗжвьЙЙЬхжаЃЌгавЛжжБНЛЗЩЯгаСНИіШЁДњЛљЧвКЫДХЙВеёЧтЦзЭМга4жжЗхЕФЮяжЪЫЕУїИУЮяжЪжаКЌга4жжЧтдзгЃЌЗћКЯЬѕМўЕФЭЌЗжвьЙЙЬхЮЊ![]() ЃЌ
ЃЌ![]() КЭNaOHШмвКдкМгШШЬѕМўЯТЗЂЩњЫЎНтЗДгІЃЌЗДгІЗНГЬЪНЮЊ
КЭNaOHШмвКдкМгШШЬѕМўЯТЗЂЩњЫЎНтЗДгІЃЌЗДгІЗНГЬЪНЮЊ![]() ЁЃ
ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ14ЗжЃЉЦћГЕЮВЦјжаCOЁЂNOxвдМАШМУКЗЯЦјжаЕФSO2ЖМЪЧДѓЦјЮлШОЮяЃЌЖдЫќУЧЕФжЮРэОпгаживЊвтвхЁЃ
ЃЈ1ЃЉбѕЛЏвЛЛЙдЗЈЯћГ§NOxЕФзЊЛЏШчЯТЃК
![]()
ЂйЗДгІIЮЊNO +O3=NO2+O2ЃЌЩњГЩБъзМзДПіЯТ11.2 L O2ЪБЃЌзЊвЦЕчзгЕФЮяжЪЕФСПЪЧ molЁЃ
ЂкЗДгІЂђжаЃЌЕБn( NO2)ЃКn[CO(NH2)2]=3ЃК2ЪБЃЌбѕЛЏВњЮягыЛЙдВњЮяЕФжЪСПБШЮЊ______
ЃЈ2ЃЉЪЙгУЁАДпЛЏзЊЛЏЦїЁБПЩвдМѕЩйЮВЦјжаЕФCOКЭNOxЃЌзЊЛЏЙ§ГЬжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊCO+ NOx ЁњN2+CO2ЃЈЮДХфЦНЃЉЃЌШєx=1.5ЃЌдђЛЏбЇЗНГЬЪНжаCO2КЭN2ЕФЛЏбЇМЦСПЪ§БШЮЊ ЁЃ
ЃЈ3ЃЉЮќЪеSO2КЭNOЃЌЛёЕУNa2S2O4КЭNH4NO3ВњЦЗЕФСїГЬЭМШчЯТЃЈCeЮЊюцдЊЫиЃЉЁЃзАжУЂђжаЃЌЫсадЬѕМўЯТЃЌNOБЛCe4+бѕЛЏЕФВњЮяжївЊЪЧNO3ЃЁЂNO2ЃЃЌЧыаДГіЩњГЩЕШЮяжЪЕФСПЕФNO3ЃКЭNO2ЃЪБЕФРызгЗНГЬЪН .

ЃЈ4ЃЉзАжУЂѓЕФзїгУжЎвЛЪЧгУжЪзгНЛЛЛФЄЕчНтВлЕчНтЪЙЕУCe4+дйЩњЃЌдйЩњЪБЩњГЩЕФCe4+дкЕчНтВлЕФ ЃЈЬюЁАбєМЋЁБЛђЁАвѕМЋЁБЃЉЃЌЭЌЪБдкСэвЛМЋЩњГЩS2O42вЛЕФЕчМЋЗДгІЪНЮЊ ЁЃ
ЃЈ5ЃЉвбжЊНјШызАжУЂєЕФШмвКжаЃЌNO2ЃЕФХЈЖШЮЊagЃЎLЃ1ЃЌвЊЪЙ1m3ИУШмвКжаЕФNO2ЃЭъШЋзЊЛЏЮЊNH4NO3ЃЌжСЩйашЯђзАжУЂєжаЭЈШЫБъзМзДПіЯТЕФбѕЦј LЃЈгУКЌaДњЪ§ЪНБэЪОЃЌНсЙћБЃСєећЪ§ЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІМШЪЧбѕЛЏЛЙдЗДгІЃЌгжЪЧЗХШШЗДгІЕФЪЧЃЈ ЃЉ
AЃЎЧтбѕЛЏФЦгыЯЁСђЫсЗДгІ
BЃЎФЦВдкCl2жаЕФШМЩе
CЃЎBaЃЈOHЃЉ28H2OгыNH4ClЕФЗДгІ
DЃЎзЦШШЕФЬПгыЫЎеєЦјЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаПЩФцЗДгІFe(s)+CO2(g)![]() FeO(s)+CO(g)ЃЌвбжЊдкЮТЖШ938KЪБЃЌЦНКтГЃЪ§K=1.5ЃЌдк1173KЪБЃЌK=2.2ЁЃ
FeO(s)+CO(g)ЃЌвбжЊдкЮТЖШ938KЪБЃЌЦНКтГЃЪ§K=1.5ЃЌдк1173KЪБЃЌK=2.2ЁЃ
(1)ФмХаЖЯИУЗДгІДяЕНЦНКтзДЬЌЕФвРОнЪЧ ЃЈЬюађКХЃЉЁЃ
AЃЎШнЦїФкбЙЧПВЛБф BЃЎcЃЈCOЃЉВЛБф
CЃЎvе§ЃЈCO2ЃЉ=vФцЃЈCOЃЉ DЃЎcЃЈCO2ЃЉ=cЃЈCOЃЉ
ЃЈ2ЃЉИУЗДгІЕФе§ЗДгІЪЧ_________ЃЈбЁЬюЁАЮќШШЁБЁЂЁАЗХШШЁБЃЉЗДгІЁЃ
(3ЃЉаДГіИУЗДгІЕФЦНКтГЃЪ§БэДяЪН__________ЁЃШєЦ№ЪМЪБАбFeКЭCO2ЗХШыЬхЛ§ЙЬЖЈЕФУмБеШнЦїжаЃЌCO2ЕФЦ№ЪМХЈЖШЮЊ2.0mol/LЃЌФГЮТЖШЪБДяЕНЦНКтЃЌДЫЪБШнЦїжаCOЕФХЈЖШЮЊ1.0 mol/LЃЌдђИУЮТЖШЯТЩЯЪіЗДгІЕФЦНКтГЃЪ§K=__________ЃЈБЃСєЖўЮЛгааЇЪ§зжЃЉЁЃ
ЃЈ4ЃЉШєИУЗДгІдкЬхЛ§ЙЬЖЈЕФУмБеШнЦїжаНјааЃЌдквЛЖЈЬѕМўЯТДяЕНЦНКтзДЬЌЃЌШчЙћИФБфЯТСаЬѕМўЃЌЗДгІЛьКЯЦјЬхжаCO2ЕФЮяжЪЕФСПЗжЪ§ШчКЮБфЛЏЃЈбЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЁАВЛБфЁБЃЉЁЃ
ЂйЩ§ИпЮТЖШ__________ЃЛЂкдйМгШыЩйСПFe___________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдк0 ЁцКЭ1ЁС105 PaЯТЃЌгУВЌЕчМЋЕчНтСђЫсЭШмвКЃЌЕБвѕМЋВњЩњ6.4 gЭЪБЃЌбєМЋЗХГі(ЁЁ )
A. 1.12 LЧтЦј B. 1.12 LбѕЦј C. 2.24 LЧтЦј D. 2.24 LбѕЦј
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП21ЪРМЭШЫРре§гЩЁАЛЏЪЏФмдДЪБДњЁБж№ВНЯђЁАЖрФмдДЪБДњЁБЙ§ЖЩЃЌЯТСаВЛЪєгкаТФмдДЕФЪЧ
AЃЎЬЋбєФм BЃЎКЫФм CЃЎЧтФм DЃЎЕчСІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдк5LЕФУмБеШнЦїжаНјааЯТЪіЗДгІ4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) 30sФкЃЌNOдіМгСЫ0ЃЎ3molЃЌдђдк30sФкЃЌИУЗДгІЕФЦНОљЗДгІЫйТЪе§ШЗЕФЪЧ
4NO(g)+6H2O(g) 30sФкЃЌNOдіМгСЫ0ЃЎ3molЃЌдђдк30sФкЃЌИУЗДгІЕФЦНОљЗДгІЫйТЪе§ШЗЕФЪЧ
AЃЎV(O2 )=0ЃЎ01molЁЄL-1ЁЄs-1 BЃЎV(NO )=0ЃЎ08molЁЄL-1ЁЄs-1
CЃЎV(H2O)=0ЃЎ01molЁЄL-1ЁЄs-1 DЃЎV(NH3)=0ЃЎ002molЁЄL-1ЁЄs-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІЪєгкЮќШШЗДгІЕФЪЧ ЃЈ ЃЉ
A. KOH +HF = KF + H2O B. CO + O2 = CO2
C. CaO + H2O = Ca(OH)2 D. NH4Cl + NaOH = NH3+ H2O +NaCl
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнЯТСаВйзїМАЯжЯѓЃЌЫљЕУГіЕФНсТле§ШЗЕФЪЧ
ађКХ | ВйзїМАЯжЯѓ | НсТл |
A | НЋжиОЇЪЏНўХндкБЅКЭЬМЫсФЦШмвКжаЃЌвЛЖЮЪБМфКѓЙЬЬхШмНт | Ksp(BaCO3)ЃМKsp(BaSO4) |
B | ЖўбѕЛЏСђЭЈШыфхЫЎжаЃЌШмвКбеЩЋЭЪШЅ | ЖўбѕЛЏСђОпгаЦЏАзад |
C | ЯђNaOHКЭNaNO3ЕФЛьКЯШмвКжаМгШыТСЗлВЂМгШШЃЌНЋЪЊШѓЕФКьЩЋЪЏШяЪджНжУгкЙмПкЃЌЪджНБфРЖ | NO3ЃЛЙдЮЊNH3 |
D | НЋ1.0molЁЄLЃ1Na2SШмвКЯЁЪЭЕН0.10molЁЄLЃ1ЃЌВтЕУpHБфаЁ | ЯЁЪЭКѓS2ЃЕФЫЎНтГЬЖШМѕаЁ |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com